Az emberek és a gerincesek egyetlen szerkezeti tervvel rendelkeznek, és a központi rész - az agy és a gerincvelő, valamint a perifériás szakasz - a központi szervekből kinyúló idegek képviselik őket, amelyek idegsejtek folyamatai - neuronok.
A neurogliasejtek jellemzői
Mint már említettük, a dendritek és axonok mielinhüvelyét speciális struktúrák alkotják, amelyekre jellemző a nátrium- és kalciumionok alacsony permeabilitása, ezért csak nyugalmi potenciáljuk van (nem vezethetnek idegimpulzusokat és nem látnak el elektromos szigetelő funkciót).
Ezeket a struktúrákat nevezzük Ezek a következők:
- oligodendrociták;
- rostos asztrociták;
- ependíma sejtek;
- plazma asztrociták.
Mindegyikük az embrió külső rétegéből - az ektodermából - jön létre, és közös neve - makroglia. A szimpatikus, paraszimpatikus és szomatikus idegek gliáját Schwann-sejtek (neurolemmociták) képviselik.
Az oligodendrociták szerkezete és funkciói
A központi idegrendszer részét képezik, és makrogliális sejtek. Mivel a mielin fehérje-lipid szerkezet, segít a gerjesztés sebességének növelésében. Maguk a sejtek az agyban és a gerincvelőben elektromosan szigetelő idegvégződésréteget alkotnak, amely már a méhen belüli fejlődés időszakában kialakul. Folyamaik a neuronokat, valamint a dendriteket és az axonokat külső plazmalemmájuk redőibe csomagolják. Kiderült, hogy a mielin a fő elektromos szigetelő anyag, amely behatárolja a kevert idegek idegfolyamatait.

és azok jellemzőit
A perifériás rendszer idegeinek mielinhüvelyét neurolemmociták (Schwann-sejtek) alkotják. Megkülönböztető jellemzőjük, hogy csak egy axonból képesek védőburkot képezni, és nem tudnak folyamatokat kialakítani, ahogy az az oligodendrocitákban rejlik.
A Schwann-sejtek között 1-2 mm távolságra vannak mielintől mentes területek, az úgynevezett Ranvier csomópontok. Rajtuk keresztül az axonon belül görcsösen elektromos impulzusokat hajtanak végre.
A lemmociták képesek javítani az idegrostokat, és teljesítenek is.A genetikai aberrációk következtében a lemmociták membránjának sejtjei kontrollálatlan mitotikus osztódásba és növekedésbe kezdenek, aminek következtében daganatok - schwannómák (neurinómák) alakulnak ki az agy különböző részein. idegrendszer.
A mikroglia szerepe a mielin szerkezet pusztításában
A mikrogliák olyan makrofágok, amelyek képesek fagocitózisra, és képesek felismerni a különféle patogén részecskéket - antigéneket. A membránreceptoroknak köszönhetően ezek a gliasejtek enzimeket - proteázokat, valamint citokineket, például interleukin 1-et termelnek. A gyulladásos folyamat és az immunitás közvetítője.
Az interleukin károsíthatja a mielinhüvelyt, amelynek feladata az axiális henger izolálása és az idegimpulzus vezetésének javítása. Ennek eredményeként az ideg "csupasz", és a gerjesztés mértéke élesen csökken.

Ezenkívül a citokinek a receptorok aktiválásával a kalciumionok túlzott transzportját provokálják a neuron testébe. A proteázok és foszfolipázok elkezdik lebontani az idegsejtek organellumait és folyamatait, ami apoptózishoz vezet - ennek a szerkezetnek a halálához.
Összeesik, részecskékre bomlik, amelyeket a makrofágok felfalnak. Ezt a jelenséget excitotoxicitásnak nevezik. A neuronok és végződéseik degenerációját okozza, ami olyan betegségekhez vezet, mint az Alzheimer-kór és a Parkinson-kór.
Pulp idegrostok
Ha a neuronok - dendritek és axonok - folyamatait mielinhüvely borítja, akkor pépesnek nevezik, és beidegzik a vázizmokat, belépve a perifériás idegrendszer szomatikus szakaszába. A nem myelinizált rostok alkotják az autonóm idegrendszert és beidegzik a belső szerveket.

A pépszerű folyamatok nagyobb átmérőjűek, mint a nem húsosak, és a következőképpen alakulnak ki: az axonok meghajlítják a gliasejtek plazmamembránját, és lineáris mezaxonokat képeznek. Ezután megnyúlnak, és a Schwann-sejtek ismételten az axon köré tekerednek, koncentrikus rétegeket képezve. A lemmocita citoplazmája és sejtmagja a külső réteg régiójába költözik, amelyet neurilemmának vagy Schwann-membránnak neveznek.
A lemmocita belső rétege réteges mezoxonból áll, és myelin hüvelynek nevezik. Vastagsága az ideg különböző részein nem azonos.
Hogyan lehet javítani a mielin hüvelyt
Figyelembe véve a mikroglia szerepét az idegi demielinizáció folyamatában, azt találtuk, hogy a makrofágok és a neurotranszmitterek (például interleukinok) hatására a mielin elpusztul, ami viszont a neuronok táplálkozásának romlásához és az átvitel megzavarásához vezet. idegimpulzusok axonok mentén.
Ez a patológia neurodegeneratív jelenségek előfordulását provokálja: a kognitív folyamatok, elsősorban a memória és a gondolkodás romlása, a testmozgások és a finom motoros készségek koordinációjának zavara.

Ennek eredményeként lehetséges a beteg teljes rokkantsága, amely autoimmun betegségek következtében következik be. Ezért a mielin helyreállításának kérdése jelenleg különösen akut. Ezek a módszerek elsősorban a kiegyensúlyozott fehérje-lipid étrendet, a megfelelő életmódot és a rossz szokások hiányát foglalják magukban. Súlyos betegségek esetén gyógyszeres kezelést alkalmaznak az érett gliasejtek - oligodendrociták - számának helyreállítására.
Az emberek és a gerincesek idegrendszere egyetlen szerkezeti tervvel rendelkezik, és a központi része - az agy és a gerincvelő, valamint a perifériás szakasz - képviseli a központi szervektől az idegek által, amelyek az idegsejtek folyamatai - az idegsejtek.
Ezek kombinációja alkotja az idegszövetet, melynek fő funkciója az ingerlékenység és a vezetőképesség. Ezeket a tulajdonságokat elsősorban a neuronok héjának szerkezeti sajátosságai és folyamataik magyarázzák, amelyek egy myelin nevű anyagból állnak. Ebben a cikkben megvizsgáljuk ennek a vegyületnek a szerkezetét és funkcióit, valamint megtudjuk a helyreállítás lehetséges módjait.
Miért borítják a neurocitákat és folyamataikat mielinnel
Nem véletlen, hogy a dendritek és axonok fehérje-lipid komplexekből álló védőréteggel rendelkeznek. A tény az, hogy a jogsértés biofizikai folyamat, amely gyenge elektromos impulzusokon alapul. Ha elektromos áram folyik át a vezetéken, akkor az utóbbit szigetelőanyaggal kell lefedni az elektromos impulzusok szétszóródásának csökkentése és az áramerősség csökkenésének megakadályozása érdekében. A mielinhüvely ugyanazokat a funkciókat látja el az idegrostokban. Ezen túlmenően, ez egy támaszték, és egyben energiát is ad a szálnak.
A mielin kémiai összetétele
A legtöbb sejtmembránhoz hasonlóan lipoprotein természetű. Ezenkívül a zsírtartalom itt nagyon magas - akár 75%, a fehérjék pedig akár 25%. A mielin kis mennyiségű glikolipidet és glikoproteineket is tartalmaz. Kémiai összetétele a gerinc- és a koponyaidegekben különbözik.
Az előbbiben magas a foszfolipidek tartalma - akár 45%, a többi pedig a koleszterinre és a cerebrozidokra esik. A demyelinizáció (vagyis a mielin más anyagokkal való helyettesítése az idegfolyamatokban) olyan súlyos autoimmun betegségekhez vezet, mint például a sclerosis multiplex.
Kémiai szempontból ez a folyamat így fog kinézni: az idegrostok mielinhüvelye megváltoztatja szerkezetét, ami elsősorban a lipidek fehérjékhez viszonyított százalékos csökkenésében nyilvánul meg. Ezenkívül csökken a koleszterin mennyisége és nő a víztartalom. Mindez pedig az oligodendrocitákat vagy Schwann-sejteket, makrofágokat, asztrocitákat és intercelluláris folyadékot tartalmazó mielin fokozatos cseréjéhez vezet. Az ilyen biokémiai változások eredménye az axonok gerjesztési képességének éles csökkenése lesz, egészen az idegimpulzusok áthaladásának teljes blokkolásához.
A neurogliasejtek jellemzői
Mint már említettük, a dendritek és axonok mielinhüvelyét speciális struktúrák alkotják, amelyeket a nátrium- és kalciumionok alacsony fokú permeabilitása jellemez, ezért csak nyugalmi potenciáljuk van (nem vezethetnek idegimpulzusokat és nem látnak el elektromos szigetelő funkciót). ). Ezeket a struktúrákat gliasejteknek nevezzük. Ezek tartalmazzák:
- oligodendrociták;
- rostos asztrociták;
- ependimális sejtek;
- plazma asztrociták.
Mindegyikük az embrió külső rétegéből - az ektodermából - jön létre, és közös neve - makroglia. A szimpatikus és paraszimpatikus szomatikus idegek gliáját Schwann-sejtek (neurolemmociták) képviselik.
Az oligodendrociták szerkezete és funkciói
A központi idegrendszer részét képezik, és makrogliális sejtek. Mivel a mielin fehérje-lipid szerkezet, segít a gerjesztés sebességének növelésében. Maguk a sejtek az agyban és a gerincvelőben elektromosan szigetelő idegvégződésréteget alkotnak, amely már a méhen belüli fejlődés időszakában kialakul. Folyamaik a neuronokat, valamint a dendriteket és az axonokat külső plazmalemmájuk redőibe csomagolják. Kiderült, hogy a mielin a fő elektromos szigetelő anyag, amely behatárolja a kevert idegek idegfolyamatait.
Schwann-sejtek és jellemzőik
A perifériás rendszer idegeinek mielinhüvelyét neurolemmociták (Schwann-sejtek) alkotják. Megkülönböztető jellemzőjük, hogy csak egy axonból képesek védőburkot képezni, és nem tudnak folyamatokat kialakítani, ahogy az az oligodendrocitákban rejlik. A Schwann-sejtek között 1-2 mm távolságra vannak mielintől mentes területek, az úgynevezett Ranvier csomópontok. Mögötte az axonon belül görcsösen elektromos impulzusok mennek végbe. A lemmociták képesek helyreállítani az idegrostokat, és trofikus funkciót is ellátnak. A genetikai aberrációk következtében a lemmocita burok sejtjeiben kontrollálatlan mitotikus osztódás és növekedés indul meg, melynek következtében az idegrendszer különböző részein daganatok, schwannómák (neurinómák) alakulnak ki.
A mikroglia szerepe a mielin szerkezet pusztításában
A mikrogliák olyan makrofágok, amelyek képesek fagocitózisra, és képesek felismerni a különféle patogén részecskéket - antigéneket. A membránreceptoroknak köszönhetően ezek a gliasejtek enzimeket - proteázokat, valamint citokineket, például interleukin 1-et termelnek. A gyulladásos folyamat és az immunitás közvetítője. Az interleukin károsíthatja a mielinhüvelyt, amelynek feladata az axiális henger izolálása és az idegimpulzus-vezetés javítása. Ennek eredményeként az ideg „ki van téve”, és a gerjesztés vezetési sebessége élesen csökken.
Ezenkívül a citokinek a receptorok aktiválásával a kalciumionok túlzott transzportját provokálják a neuron testébe. A proteázok és foszfolipázok elkezdik lebontani az idegsejtek organellumait és folyamatait, ami apoptózishoz vezet - ennek a szerkezetnek a halálához. Összeesik, részecskékre bomlik, amelyeket a makrofágok felfalnak. Ezt a jelenséget excitotoxicitásnak nevezik. A neuronok és végződéseik degenerációját okozza, ami olyan betegségekhez vezet, mint az Alzheimer-kór és a Parkinson-kór.
Pulp idegrostok
Ha a neuronok - dendritek és axonok - folyamatait mielinhüvely borítja, akkor pépesnek nevezik, és beidegzik a vázizmokat, belépve a perifériás idegrendszer szomatikus szakaszába. A nem myelinizált rostok alkotják az autonóm idegrendszert és beidegzik a belső szerveket.
A pulpos folyamatok nagyobb átmérőjűek, mint a nem pulmonális folyamatok, és a következőképpen alakulnak ki: az axonok meghajlítják a gliasejtek plazmamembránját, és lineáris mezaxonokat képeznek. Ezután megnagyobbodnak, és a Schwann-sejtek ismételten az axon köré tekerednek, koncentrikus rétegeket képezve. A lemmocita citoplazmája és sejtmagja a külső réteg régiójába költözik, amelyet neurilemmának vagy Schwann-membránnak neveznek. A lemmocita belső rétege réteges mezoxonból áll, és myelin hüvelynek nevezik. Vastagsága az ideg különböző részein nem azonos.
Hogyan lehet javítani a mielin hüvelyt
Figyelembe véve a mikroglia szerepét az idegi demielinizáció folyamatában, azt találtuk, hogy a makrofágok és a neurotranszmitterek (például interleukinok) hatására a mielin elpusztul, ami viszont a neuronok táplálkozásának romlásához és a transzmisszió megsértéséhez vezet. idegimpulzusok axonok mentén. Ez a patológia neurodegeneratív jelenségek előfordulását provokálja: a kognitív folyamatok, elsősorban a memória és a gondolkodás romlása, a testmozgások és a finom motoros készségek koordinációjának zavara.
Ennek eredményeként lehetséges a beteg teljes rokkantsága, amely autoimmun betegségek következtében következik be. Ezért a mielin helyreállításának kérdése jelenleg különösen akut. Ezek a módszerek elsősorban a kiegyensúlyozott fehérje-lipid étrendet, a megfelelő életmódot és a rossz szokások hiányát foglalják magukban. Súlyos betegségek esetén gyógyszeres kezelést alkalmaznak az érett gliasejtek - oligodendrociták - számának helyreállítására.
Megjelenés dátuma: 05/26/17A központi idegrendszer (CNS) egyetlen mechanizmus, amely felelős a környező világ észleléséért és a reflexekért, valamint a belső szervek és szövetek rendszerének szabályozásáért. Az utolsó pontot a központi idegrendszer perifériás része hajtja végre speciális sejtek, úgynevezett neuronok segítségével. Ezekből áll az idegszövet, amely impulzusok továbbítására szolgál.
Az idegsejt testéből érkező folyamatokat az idegrostokat tápláló, az impulzusok átvitelét felgyorsító védőréteg veszi körül, az ilyen védelmet myelinhüvelynek nevezik. Az idegrostokon keresztül továbbított bármely jel az áramkisüléshez hasonlít, és a külső rétegük nem engedi, hogy az erőssége csökkenjen.
Ha a mielinhüvely megsérül, akkor a test ezen részén a teljes érzékelés megszűnik, de a sejt túléli, és a károsodás idővel gyógyul. Megfelelően súlyos sérülések esetén az idegrostok helyreállítására tervezett gyógyszerekre lesz szükség, mint például a Milgamma, a Copaxone és mások. Ellenkező esetben az ideg végül meghal, és az észlelés csökken. A problémával jellemezhető betegségek közé tartozik a radiculopathia, polyneuropathia stb., de az orvosok a sclerosis multiplexet (SM) tartják a legveszélyesebb kóros folyamatnak. A furcsa név ellenére a betegségnek semmi köze e szavak közvetlen meghatározásához, és fordításban "több heget" jelent. A gerincvelőben és az agyban az immunrendszer elégtelensége miatt a mielinhüvelyen fordulnak elő, így az SM egy autoimmun betegség. Az idegrostok helyett a fókusz helyén kötőszövetből álló heg jelenik meg, amelyen már nem tud megfelelően áthaladni az impulzus.
Lehetséges valahogyan helyreállítani a sérült idegszövetet, vagy örökre megnyomorodott állapotban marad? Az orvosok még mindig nem tudnak erre pontosan válaszolni, és még nem dolgoztak ki teljes értékű gyógyszert az idegvégződésekkel szembeni érzékenység helyreállítására. Ehelyett léteznek különféle gyógyszerek, amelyek csökkenthetik a demyelinizációs folyamatot, javíthatják a sérült területek táplálkozását és aktiválhatják a mielinhüvely regenerálódását.
A Milgamma egy neuroprotektor a sejten belüli anyagcsere helyreállítására, amely lehetővé teszi a mielin pusztulási folyamatának lelassítását és regenerációjának elindítását. A gyógyszer a B csoportba tartozó vitaminokon alapul, nevezetesen:
- Tiamin (B1). Elengedhetetlen a cukor szervezetben történő felszívódásához és az energiához. Akut tiaminhiány esetén az alvás zavart szenved, és a memória romlik. Ideges lesz, és néha depressziós lesz, mint a depresszióban. Egyes esetekben paresztézia tünetei vannak (libabőr, csökkent érzékenység és bizsergés az ujjbegyekben);
- Piridoxin (B6). Ez a vitamin fontos szerepet játszik az aminosavak, valamint egyes hormonok (dopamin, szerotonin stb.) termelésében. Annak ellenére, hogy ritka esetekben hiányzik a piridoxin a szervezetben, annak hiánya miatt a mentális képességek csökkenése és az immunvédelem gyengülése lehetséges;
- Cianokobalamin (B12). Az idegrostok vezetőképességének javítására szolgál, ami javítja az érzékenységet, valamint javítja a vérszintézist. A cianokobalamin hiányában hallucinációk, demencia (demencia) alakulnak ki, szívritmuszavarok és paresztézia lép fel.
Ennek az összetételnek köszönhetően a Milgama képes megállítani a sejtek szabad gyökök (reaktív anyagok) általi oxidációját, ami befolyásolja a szövetek és idegvégződések érzékenységének helyreállítását. A tabletták szedése után a tünetek csökkenése és az általános állapot javulása következik be, és a gyógyszert 2 szakaszban kell bevenni. Az elsőben legalább 10 injekciót kell beadnia, majd át kell váltania a tablettákra (Milgamma compositum), és naponta háromszor kell bevennie őket 1,5 hónapig.

A sztafaglabrin-szulfátot régóta használják a szövetek és maguk az idegrostok érzékenységének helyreállítására. A növény, amelynek gyökereiből ezt a gyógyszert kivonják, csak szubtrópusi és trópusi éghajlaton nő, például Japánban, Indiában és Burmában, és Stephania smooth-nak nevezik. Vannak esetek, amikor a Stafaglabrin-szulfátot laboratóriumban nyerik. Talán ez annak a ténynek köszönhető, hogy a stephania smooth szuszpenziós kultúraként, azaz felfüggesztett helyzetben, folyadékkal ellátott üveglombikban termeszthető. Önmagában a gyógyszer egy szulfátsó, amelynek magas olvadáspontja van (több mint 240 ° C). Ez az alkaloid (nitrogéntartalmú vegyület) sztefarinra utal, amelyet a proaporfin alapjának tekintenek.
A sztefaglabrin-szulfát a hidrolázok (kolinészteráz) osztályába tartozó enzimek aktivitásának csökkentésére, valamint az erek falában, a szervekben (belül üreges) és a nyirokcsomókban található simaizmok tónusának javítására szolgál. Az is ismert, hogy a gyógyszer enyhén mérgező, és csökkentheti a vérnyomást. A régi időkben a gyógyszert antikolinészteráz szerként használták, de aztán a tudósok arra a következtetésre jutottak, hogy a Stefaglabrin-szulfát a kötőszövet növekedési aktivitásának inhibitora. Ebből kiderül, hogy késlelteti a fejlődését és nem keletkeznek hegek az idegrostokon. Ezért kezdték aktívan használni a gyógyszert a PNS károsodására.
A kutatás során a szakértőknek a perifériás idegrendszerben mielint termelő Schwann-sejtek növekedését láthatták. Ez a jelenség azt jelenti, hogy a gyógyszer hatására a beteg észrevehetően javítja az impulzus vezetését az axon mentén, mivel a mielinhüvely ismét elkezdett kialakulni körülötte. Az eredmények megszerzése óta a gyógyszer sok olyan ember reményévé vált, akiknél gyógyíthatatlan demyelinizációs patológiát diagnosztizáltak.

Az autoimmun patológia problémáját nem lehet csak az idegrostok helyreállításával megoldani. Valóban, akárhány károsodási gócot kell megszüntetni, a probléma visszatér, hiszen az immunrendszer idegen testként reagál a mielinre, és elpusztítja azt. A mai napig lehetetlen kiküszöbölni egy ilyen kóros folyamatot, de már nem lehet csodálkozni azon, hogy az idegrostok helyreálltak-e vagy sem. Az embereknek meg kell őrizniük állapotukat azáltal, hogy elnyomják az immunrendszert, és olyan gyógyszereket használnak, mint a Stefaglabrin-szulfát egészségük megőrzése érdekében.
A gyógyszer csak parenterálisan, azaz a belekben, például injekció formájában alkalmazható. Az adag ebben az esetben nem haladhatja meg a napi 7-8 ml 0,25%-os oldatot 2 injekcióhoz. Időből ítélve a mielinhüvely és az idegvégződések általában 20 nap elteltével helyreállnak valamennyire, és akkor kell egy kis szünet, és az orvostól megtudva érthető, meddig tart. Az orvosok szerint a legjobb eredményt az alacsony dózisok rovására lehet elérni, mivel a mellékhatások sokkal ritkábban alakulnak ki, és a kezelés hatékonysága nő.
Laboratóriumi körülmények között, a patkányokon végzett kísérletek idején azt találták, hogy a Stefaglabrin-szulfát gyógyszer 0,1-1 mg / kg koncentrációjával a kezelés gyorsabb, mint anélkül. A terápia folyamata korábban véget ért, összehasonlítva azokkal az állatokkal, amelyek nem szedték ezt a gyógyszert. 2-3 hónap elteltével a rágcsálókban az idegrostok szinte teljesen helyreálltak, és az impulzus késedelem nélkül továbbhaladt az ideg mentén. Azoknál a kísérleti alanyoknál, akiket e gyógyszer nélkül kezeltek, a gyógyulás körülbelül hat hónapig tartott, és nem minden idegvégződés tért vissza a normális állapotba.
Copaxone

A sclerosis multiplexre nincs gyógymód, de vannak olyan gyógyszerek, amelyek csökkenthetik az immunrendszer myelinhüvelyre gyakorolt hatását, ezek közé tartozik a Copaxone is. Az autoimmun betegségek lényege, hogy az immunrendszer elpusztítja az idegrostokon található mielint. Emiatt az impulzusok vezetőképessége romlik, és a Copaxone képes a szervezet védekezőrendszerének célját önmagára változtatni. Az idegrostok érintetlenek maradnak, de ha a szervezet sejtjei már felvették a mielinhüvely erózióját, akkor a gyógyszer képes lesz visszaszorítani őket. Ez a jelenség abból adódik, hogy a gyógyszer szerkezetében nagyon hasonló a mielinhez, így az immunrendszer ráirányítja a figyelmét.
A gyógyszer nemcsak a szervezet védekezőrendszerének támadását képes felvenni, hanem a betegség intenzitásának csökkentésére az immunrendszer speciális sejtjeit is termeli, amelyeket Th2-limfocitáknak neveznek. Befolyásuk és kialakulásának mechanizmusát még nem vizsgálták megfelelően, de különféle elméletek léteznek. A szakértők véleménye szerint az epidermisz dendrites sejtjei részt vesznek a Th2-limfociták szintézisében.
A kialakult szuppresszor (mutált) limfociták a vérbe kerülve gyorsan behatolnak az idegrendszer azon részébe, ahol a gyulladás fókusza található. Itt a Th2 limfociták a mielin hatására citokineket, azaz gyulladásgátló molekulákat termelnek. Elkezdik fokozatosan enyhíteni a gyulladást az agy ezen részén, ezáltal javítva az idegvégződések érzékenységét.
A gyógyszer előnyei nemcsak magának a betegségnek a kezelésére, hanem magukra az idegsejtekre is vonatkoznak, mivel a Copaxone neuroprotektor. A védőhatás az agysejtek növekedésének serkentésében és a lipidanyagcsere javításában nyilvánul meg. A mielinhüvely főleg lipidekből áll, és számos, az idegrostok károsodásával járó kóros folyamatban ezek oxidációja következik be, így a mielin károsodik. A Copaxone gyógyszer képes kiküszöbölni ezt a problémát, mivel növeli a szervezet természetes antioxidánsát (húgysav). Nem ismert, hogy mitől emelkedik a húgysav szintje, de ezt a tényt számos kísérlet során igazolták.
A gyógyszer az idegsejtek védelmét és az exacerbációk súlyosságának és gyakoriságának csökkentését szolgálja. Kombinálható a Stefaglabrin-szulfát és a Milgamma gyógyszerekkel.
A mielinhüvely a Schwann-sejtek fokozott növekedése miatt kezd helyreállni, a Milgamma pedig javítja az intracelluláris anyagcserét és fokozza mindkét gyógyszer hatását. Szigorúan tilos önmagukban használni őket, vagy önmagukban megváltoztatni az adagolást.
Lehetséges-e az idegsejtek helyreállítása, és mennyi ideig tart, csak szakember válaszolhat, a vizsgálat eredményeire összpontosítva. Tilos bármilyen gyógyszert önállóan bevenni a szövetek érzékenységének javítására, mivel ezek többsége hormonális alapokon nyugszik, ami azt jelenti, hogy a szervezet nehezen tolerálja őket.
IDEGROSTOK
Az idegrostok gliahüvellyel borított neuronok folyamatai. Kétféle idegrost létezik - myelinizált és myelinizált. Mindkét típus egy neuron (axiális henger) centrálisan fekvő folyamatából áll, amelyet oligodendroglia sejtek (a PNS-ben lemmocitáknak vagy Schwann-sejteknek) vesznek körül.
nem myelinizált idegrostok felnőtteknél főként az autonóm idegrendszerben helyezkednek el, és viszonylag alacsony idegimpulzus-vezetési sebesség jellemzi őket (0.5-2 Kisasszony). Úgy jönnek létre, hogy az axiális hengert (axont) a lemmociták citoplazmájába merítik, amelyek szálak formájában helyezkednek el. Ebben az esetben a lemmocita plazmolemmája meggörbül, körülveszi az axont, és duplikációt képez - a mezaxont (2. 14-7). Egy-egy lemmocita citoplazmájában gyakran akár 10-20 tengelyhengerek. Az ilyen szál elektromos kábelre hasonlít, ezért kábel típusú szálnak nevezik. A rost felületét alapmembrán borítja. A központi idegrendszerben, különösen annak fejlődése során, nem myelinizált rostokat írnak le, amelyek egy "csupasz" axonból állnak, és nem tartalmaznak lemmociták burkot.
Rizs. 14-7. Myelinizált (1-3) és nem myelinizált (4) idegrostok kialakulása a perifériás idegrendszerben. Az idegrost úgy jön létre, hogy az idegsejt axonját (A) a lemmocita (LC) citoplazmájába merítik. Amikor mielinrost képződik, az LC plazmolemma duplikációja - mezaxon (MA) - tekercselődik az A körül, és a mielinhüvely (MO) fordulatait képezi. Az ábrán látható mielinmentes rostban az LC (kábel típusú rost) citoplazmájában több A is elmerül. Én vagyok az LC magja.

myelinizált idegrostok a központi idegrendszerben és a PNS-ben találhatók, és nagy sebességű idegimpulzus-vezetés jellemzi őket (5-120 Kisasszony). A myelinizált rostok általában vastagabbak, mint a nem myelinizáltak, és nagyobb átmérőjű axiális hengereket tartalmaznak. A mielinrostban az axiális hengert közvetlenül körülveszi egy speciális mielinhüvely, amely körül egy vékony réteg található, amely magában foglalja a citoplazmát és a lemmocita magját - a neurolemma. 14-8 és 14-9). Kívül a szálat alapmembrán is borítja. A mielinhüvely magas koncentrációban tartalmaz lipideket és intenzíven festődik ozmossavval, fénymikroszkóp alatt homogén rétegnek tűnik, de elektronmikroszkóp alatt azt találják, hogy számos (akár 300) membrántekercsek (lemezek).
Rizs. 14-8. A myelinizált idegrost szerkezete. A mielinrost egy axiális hengerből vagy axonból (A) áll, amelyet közvetlenül egy mielinhüvely (MO) és egy neurolemma (NL) vesz körül, beleértve a citoplazmát (CL) és a lemmocyta magot (NL). Kívül a szálat alapmembrán (BM) borítja. Az MO azon területei, amelyekben a mielinfordulatok közötti rések megmaradtak, CL-vel kitöltve, ezért nem festődnek ozmiummal, myelin rovátkák (MN) formájúak.
Mielinhüvely kialakulása Az axiális henger és az oligodendroglia sejtek kölcsönhatása során fordul elő, a PNS és a CNS bizonyos eltéréseivel.
Mielinhüvely kialakulása a PNS-ben : az axiális henger bemerülése a lemmocitába egy hosszú mezaxon képződésével jár együtt, amely az axon körül forogni kezd, kialakítva a myelinhüvely első lazán elrendezett fordulatait (lásd 1. ábra). 14-7). Ahogy a myelin érésének folyamatában a fordulatok (lemezek) száma növekszik, egyre sűrűbben helyezkednek el és részben összeolvadnak; a köztük lévő, a lemmocita citoplazmájával kitöltött rések csak különálló területeken maradnak meg, amelyek nem festettek ozmium-myelin bevágásokkal (Schmidt-Lanterman). A mielinhüvely kialakulása során a citoplazma és a lemmocita magja a rost perifériájára szorul, kialakítva a neurolemmát. A mielinhüvely szakaszos lefolyású a rost hosszában.

Rizs. 14-9. A myelinizált idegrost ultrastrukturális szerveződése. Az axon (A) körül a mielinhüvely (MMO) tekercsei találhatók, amelyet kívülről neurolemma borít, és amely magában foglalja a citoplazmát (CL) és a lemmocyta magját (NL). A szálat kívülről alapmembrán (BM) veszi körül. A CL a neurolemmán kívül egy belső lapot (IL) képez közvetlenül az A mellett (amely közte és az SMO között helyezkedik el), és a szomszédos lemmociták határának megfelelő zónában is található - a csomópont elfogása (NC), ahol a mielinhüvely hiányzik, és a laza WMO-halmozódású területeken - myelin rovátkák (MN).
Csomóponti elfogások (Ranvier)- a szomszédos lemmociták határának régiójában található területek, ahol a mielinhüvely hiányzik, és az axont csak a szomszédos lemmociták interdigitáló folyamatai fedik le (lásd 14-9. ábra). A csomópontok elfogása a mielinrost lefutása mentén megismétlődik, átlagosan 1-2 mm-rel. A csomópont régiójában az axon gyakran kitágul, és plazmolemmája számos nátriumcsatornát tartalmaz (amelyek a myelin hüvely alatti csomópontokon kívül hiányoznak).
A depolarizáció terjedése a mielinrostban ugrásokban hajtják végre az elfogástól az elfogásig (sózó). Az egyik csomópont régiójában a depolarizáció gyors passzív terjedésével jár az axon mentén a következő csomópontig (mivel az internodális régióban az áramszivárgás minimális a mielin magas szigetelő tulajdonságai miatt). A következő metszéspont területén az impulzus hatására a meglévő ioncsatornák bekapcsolnak, és megjelenik a helyi depolarizáció új területe stb.
Mielinhüvely kialakulása a központi idegrendszerben: az axiális henger nem süllyed az oligodendrocita citoplazmájába, hanem lapos folyamata borítja, amely ezt követően körülötte forog, elveszti a citoplazmát, és tekercsei a mielinhüvely lemezeivé alakulnak

könyökök (14-10. ábra). A Schwann sejtekkel ellentétben egy központi idegrendszeri oligodendrocita folyamataival számos (akár 40-50) idegrost myelinizációjában is részt vehet. A központi idegrendszerben a Ranvier csomópontjainak területén található axonhelyeket nem fedi le az oligodendrociták citoplazmája.
Rizs. 14-10. Myelin rostok képződése oligodendrociták által a központi idegrendszerben. 1 - a neuron axonját (A) az oligodendrocita (ODC) lapos folyamata (PO) fedi, amelynek tekercsei a mielinhüvely (MO) lemezeivé alakulnak. 2 - egy ODC a folyamataival részt vehet számos A mielinizációjában. A csomópontok (NC) területén lévő A területeket nem fedi le az ODC citoplazmája.
A kialakult mielin képződésének és károsodásának megsértése számos súlyos idegrendszeri betegség hátterében áll. A központi idegrendszerben található mielin az autoimmun károsodás célpontja lehet T-limfociták a makrofágok pedig annak elpusztításával (demielinizáció). Ez a folyamat aktívan megy végbe a sclerosis multiplexben, egy súlyos, tisztázatlan (valószínűleg vírusos) természetű betegségben, amely különböző funkciók zavarával, bénulás kialakulásával és érzékenységvesztéssel jár. A neurológiai rendellenességek természetét a sérült területek domborzata és mérete határozza meg. Egyes anyagcsere-rendellenességek esetén a mielin képződésében - leukodystrophia - rendellenességek lépnek fel, amelyek gyermekkorban az idegrendszer súlyos elváltozásaiban nyilvánulnak meg.
Az idegrostok osztályozása
Az idegrostok osztályozása szerkezetükben és működésükben (az idegimpulzusok sebességében) lévő különbségeken alapul. Az idegrostok három fő típusa van:
1. A típusú szálak - vastag, mielinizált, távoli csomóponti elfogásokkal. Vezessen impulzusokat nagy sebességgel
(15-120 m/s); 4 altípusra (α, β, γ, δ) oszlik, amelyek átmérője és impulzusvezetési sebessége csökken.
2. B típusú rostok - közepes vastagságú, mielin, kisebb átmérőjű,
mint az A típusú rostok, vékonyabb mielinhüvellyel és alacsonyabb idegimpulzus-vezetési sebességgel (5-15 m/s).
3. C típusú rostok - vékony, nem myelinizált, viszonylag kis sebességgel vezetnek impulzusokat(0,5-2 m/s).
Az idegrostok regenerációja a PNS-ben magában foglalja a folyamatok természetesen kibontakozó összetett sorozatát, amely során a neuronfolyamat aktívan kölcsönhatásba lép a gliasejtekkel. A szálak tényleges regenerációja a károsodásuk által okozott reaktív változások sorozatát követi.
Reaktív változások az idegrostban annak átmetszése után. Az idegrost átvágását követő 1. héten az axon proximális (a neuron testéhez legközelebb eső) részének felszálló degenerációja alakul ki, melynek végén extenzió (retrakciós lombik) képződik. A károsodás területén a mielinhüvely felbomlik, a neuron teste megduzzad, a sejtmag a perifériára tolódik, a kromatofil anyag feloldódik (14-11. ábra).
A rost disztális részén, annak átmetszése után, csökkenő degeneráció figyelhető meg az axon teljes pusztulásával, a mielin lebomlásával, majd a detritus makrofágok és glia által történő fagocitózisával.
Szerkezeti átalakulások az idegrost regenerációja során. 4-6 hét után. helyreáll a neuron szerkezete és működése, a visszahúzó lombikból vékony ágak (növekedési kúpok) kezdenek növekedni a rost disztális része irányába. A rost proximális részében a Schwann-sejtek szaporodnak, és a rost lefutásával párhuzamos szalagokat (Büngner) képeznek. A rost disztális részében a Schwann-sejtek is fennmaradnak és mitotikusan osztódnak, szalagokat képezve, amelyek a proximális rész hasonló képződményeihez kapcsolódnak.
A regenerálódó axon disztális irányban 3-4 mm/nap sebességgel nő. a támogató és irányító szerepet játszó Büngner-szalagok mentén; A Schwann-sejtek új mielinhüvelyt képeznek. A biztosítékok és az axonterminálok néhány hónapon belül helyreállnak.

Rizs. 14-11. A myelinizált idegrost regenerációja (R.Krstic szerint, 1985, változásokkal). 1 - az idegrost átmetszése után az axon (A) proximális része felszálló degeneráción megy keresztül, a károsodás területén a mielinhüvely (MO) felbomlik, a neuron perikarionja (PC) megduzzad, a mag eltolódik a perifériára a kromatofil anyag (CS) szétesik (2). A beidegzett szervhez kapcsolódó disztális rész (az adott példában a vázizomzat) lefelé degenerálódik, az A teljes pusztulásával, az MO szétesésével és a detritus makrofágok (MF) és glia fagocitózisával. A lemmociták (LC) fennmaradnak és mitotikusan osztódnak, szálakat képezve - Büngner-szalagokat (LB), amelyek hasonló képződményekhez kapcsolódnak a rost proximális részében (vékony nyilak). 4-6 hét elteltével a neuron szerkezete és funkciója helyreáll, vékony ágak nőnek disztálisan az A proximális résztől (félkövér nyíl), az LB mentén nőnek (3). Az idegrost regenerációja következtében helyreáll a kapcsolat a célszervvel (izomzattal), és visszafejlődik a károsodott beidegzés okozta sorvadás (4). Abban az esetben, ha elzáródás (P) a regenerálódó A útján (például kötőszöveti heg), az idegrost összetevői
traumás neuromát (TN) alkotnak, amely növekvő A és LC ágakból áll (5).
regenerációs feltételek a következők: nincs károsodás a neuron testében, kis távolság az idegrost részei között, hiányzik a kötőszövet, amely kitöltheti a rost részei közötti rést. Ha a regenerálódó axon útjában elzáródás lép fel, traumás (amputációs) neuroma képződik, amely növekvő axonból és a kötőszövetbe forrasztott Schwann-sejtekből áll.
A központi idegrendszerben nincs idegrostok regenerációja : bár a központi idegrendszeri neuronok képesek visszaállítani folyamataikat, ez nem történik meg, látszólag a mikrokörnyezet káros hatása miatt. Egy neuron károsodása után a mikroglia, az asztrociták és a hematogén makrofágok fagocitizálják a törmeléket az elpusztult rost területén, és a burjánzó asztrociták sűrű glia heget képeznek a helyén.
IDEGVÉGZŐDÉSEK
Idegvégződések- idegrostok végberendezései. Funkciójuk szerint három csoportra oszthatók:
1) interneuronális kontaktusok (szinapszisok)- funkcionális kapcsolatot biztosítanak az idegsejtek között;
2) efferens (effektor) végződések- jeleket továbbít az idegrendszerből a végrehajtó szervekbe (izmok, mirigyek), jelen vannak az axonokon;
3) receptor (érzékeny) végződésekkülső és belső környezetből származó irritációt észlel, jelen van a dendriten.
INTERNEURONÁLIS KAPCSOLATOK (SZINAPSZIS)
Interneuronális érintkezések (szinapszisok) elektromos és vegyi részekre osztva.
elektromos szinapszisok emlősök központi idegrendszerében ritka; gap junctions szerkezetűek, amelyekben a szinaptikusan összefüggő (pre- és posztszinaptikus) sejtek membránjait egy 2 nm széles, konnexonokkal áttört rés választja el. Ez utóbbiak fehérjemolekulák által alkotott csövek, és vízcsatornaként szolgálnak, amelyeken keresztül kis molekulák és ionok szállíthatók egyik sejtből a másikba.

egy másik (lásd a 3. fejezetet). Amikor az egyik sejt membránján átterjedő akciós potenciál eléri a réspontot, az elektromos áram passzívan áramlik át a résen egyik sejtből a másikba. Az impulzus mindkét irányban és gyakorlatilag késleltetés nélkül továbbítható.
Kémiai szinapszisok- emlősökben a leggyakoribb típus. Működésük azon alapul, hogy egy elektromos jelet kémiai jellé alakítanak át, amely aztán visszaalakul elektromos jellé. A kémiai szinapszis három komponensből áll: a preszinaptikus részből, a posztszinaptikus részből és a szinaptikus hasadékból (14-12. ábra). A preszinaptikus rész egy (neuro)transzmittert tartalmaz, amely idegimpulzus hatására a szinaptikus hasadékba kerül, és a posztszinaptikus rész receptoraihoz kötődve megváltoztatja membránjának ionáteresztő képességét, ami a depolarizáció (serkentő szinapszisokban) vagy hiperpolarizáció (gátló szinapszisokban). A kémiai szinapszisok különböznek az elektromos szinapszisoktól az impulzusok egyoldalú vezetésében, átvitelük késleltetésében (0,2-0,5 ms szinaptikus késleltetés), valamint a posztszinaptikus neuron gerjesztésében és gátlásában.
Rizs. 14-12. A kémiai szinapszis szerkezete. A preszinaptikus rész (PRSP) terminális gomb (CB) alakú, és a következőket tartalmazza: szinaptikus vezikulák (SP), mitokondriumok (MTX), neurotubulusok (NT), neurofilamentumok (NF), preszinaptikus membrán (PRSM) preszinaptikus tömörítéssel (PRSU) ). A posztszinaptikus rész (PSCH) tartalmazza a posztszinaptikus membránt (POSM) a posztszinaptikus tömörítéssel (POSU). A szinaptikus hasadék (SC) intraszinaptikus filamentumokat (ISF) tartalmaz.
1. preszinaptikus rész az axon a pályája mentén alkotja (áthaladó szinapszis), vagy az axon kiterjesztett végrésze (terminális bimbó). 20-65 nm átmérőjű mitokondriumokat, aER-t, neurofilamentumokat, neurotubulusokat és szinaptikus vezikulákat tartalmaz, amelyek a neurotranszmittert tartalmazzák. A hólyagok tartalmának alakja és jellege a bennük lévő neurotranszmitterektől függ. A kerek, világos vezikulák általában acetilkolint, tömör, sűrű központú vezikulákat - noradrenalint, nagy, sűrű vezikulákat könnyű submembrán peremmel - peptideket tartalmaznak. A neurotranszmitterek az idegsejt testében termelődnek, és a gyors transzport mechanizmusával az axonvégződésekhez kerülnek, ahol lerakódnak. Részben szinaptikus vezikulák képződnek magában a szinapszisban az aER ciszternáiból kiválva. A plazmolemma belső oldalán, a szinaptikus hasadékkal (preszinaptikus membrán) szemben, egy fibrilláris hexagonális fehérjehálózat alkotta preszinaptikus tömítés található, amelynek sejtjei hozzájárulnak a szinaptikus vezikulák egyenletes eloszlásához a membrán felületén.
2. posztszinaptikus rész Egy posztszinaptikus membrán képviseli, amely integrált fehérjék speciális komplexeit tartalmazza - szinaptikus receptorok, amelyek egy neurotranszmitterhez kötődnek. A membrán megvastagszik az alatta lévő sűrű fonalas fehérjeanyag (posztszinaptikus tömörítés) miatt. Attól függően, hogy az interneuronális szinapszis posztszinaptikus része a dendrit, a neuron teste vagy (ritkábban) az axonja, a szinapszisokat axo-dendrites, axosomatikus és axoaxonálisra osztják.
3. szinaptikus hasadék 20-30 nm széles, esetenként 5 nm vastagságú transzverzális glikoprotein intraszinaptikus filamentumokat tartalmaz, amelyek egy speciális glikokalix elemei, amelyek a pre- és posztszinatikus részek tapadó kötéseit, valamint a mediátor irányított diffúzióját biztosítják.
Az idegimpulzus átvitelének mechanizmusa kémiai szinapszisban. Idegimpulzus hatására a preszinaptikus membrán feszültségfüggő kalciumcsatornái aktiválódnak; Sa 2+ az axonhoz rohan, a szinaptikus vezikulák membránjai Ca2+ jelenlétében egyesülnek a preszinaptikus membránnal, és tartalmuk (közvetítő) exocitózis mechanizmusával a szinaptikus hasadékba kerül. A mediátor a posztszinaptikus membrán receptoraira hatva vagy annak depolarizációját, posztszinaptikus akciós potenciál kialakulását és idegimpulzus képződését, vagy hiperpigmentációját idézi elő.
polarizáció, gátló választ okozva. A serkentő mediátorok például az acetilkolin és a glutamát, míg a gátlást a GABA és a glicin közvetíti.
A mediátor és a posztszinaptikus membrán receptoraival való kölcsönhatásának megszűnése után endocitózisának nagy részét a preszinaptikus rész, a kisebb részt a térben szétszórva a környező gliasejtek rögzítik. Egyes mediátorokat (például az acetilkolint) az enzimek komponensekre bontják, amelyeket aztán a preszinaptikus rész felfog. A preszinaptikus membránba ágyazott szinaptikus vezikulum membránokat tovább építik be az endocitikus bélésű vezikulákba, és újra felhasználják új szinaptikus vezikulák képzésére.
Idegimpulzus hiányában a preszinaptikus rész felszabadítja a mediátor egyes kis részeit, ami spontán miniatűr potenciálokat okoz a posztszinaptikus membránban.
EFFERENT (EFFEKTOR) Idegvégződések
Efferens (effektor) idegvégződések A beidegzett szerv természetétől függően motoros és szekréciós részekre oszthatók. Motorvégződések a harántcsíkolt és simaizmokban, a szekréciós - a mirigyekben találhatók.
Neuromuszkuláris végződés (neuromuszkuláris csomópont, motoros plakk) - a motoros neuron axonjának motoros végződése a harántcsíkolt szomatikus izmok rostjain - a preszinaptikus részt alkotó axon terminális elágazásából, az izomroston egy, a posztszinaptikus résznek megfelelő speciális területből áll, ill. az őket elválasztó szinaptikus hasadék (ábra). 14-13).
Jelentős erőt fejlesztő nagy izmokban egy axon elágazóan nagyszámú (száz és ezer) izomrostot beidegz be. Éppen ellenkezőleg, a finom mozdulatokat végző kis izmokban (például a szem külső izmaiban) minden rostot vagy azok egy kis csoportját külön axon beidegzi. Az egyik motoros neuron az általa beidegzett izomrostokkal együtt motoros egységet alkot.
preszinaptikus rész. Az izomrost közelében az axon elveszti mielinhüvelyét, és több ágat hoz létre, amelyek
A sclerosis multiplex egy újabb bizonyítéka immunrendszerünk tökéletlenségének, amely időnként „megőrül”, és nem egy külső „ellenséget”, hanem saját testének szöveteit kezdi megtámadni. Ebben a betegségben az immunrendszer sejtjei elpusztítják az idegrostok mielinhüvelyét, amely a test fejlődése során képződik bizonyos típusú gliasejtekből - az idegrendszer "szolgálati" sejtjeiből. A mielinhüvely axonokat takar - egy neuron hosszú folyamatait, amelyek "huzalként" működnek, amelyen keresztül az idegimpulzus halad. Maga a hüvely elektromos szigetelésként szolgál, és megsemmisülése következtében az idegrost mentén 5-10-szeresére lelassul az impulzus áthaladása.
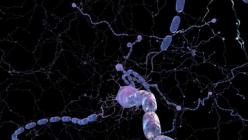
A képen a makrofágok (barna színű) felhalmozódása látható a plakkok perifériáján. A makrofágokat a lézió vonzza, és az immunrendszer más sejtjei - a T-limfociták - aktiválják. Az aktivált makrofágok fagocitizálják ("eszik") a haldokló mielint, ráadásul ők maguk is hozzájárulnak annak károsodásához, proteázokat, gyulladást elősegítő molekulákat és reaktív oxigénfajtákat termelve. (Immunhisztokémia, makrofág marker - CD68).
Normális esetben az immunrendszer sejtjei más vérsejtekhez hasonlóan nem képesek közvetlenül behatolni az idegszövetbe – az úgynevezett vér-agy gát nem engedi őket. A szklerózis multiplex esetén azonban ez a gát átjárhatóvá válik: az „őrült” limfociták hozzáférnek a neuronokhoz és azok axonjaihoz, ahol megtámadják a mielinmolekulákat, amelyek egy összetett többrétegű fehérje-lipid szerkezet. Ez molekuláris események sorozatát indítja el, amelyek a mielin és néha maguk az axonok pusztulásához vezetnek.
A mielin pusztulását az érintett terület gyulladásának és szklerózisának kialakulása kíséri, i.e. kötőszöveti heg kialakulása plakk formájában, amely a mielinhüvelyt helyettesíti. Ennek megfelelően ezen a területen az axon vezető funkciója károsodik. A plakkok diffúzan helyezkednek el, szétszórva az idegrendszerben. Az elváltozások ilyen elrendezéséhez kapcsolódik a betegség neve is - „szklerózis multiplex”, amelynek semmi köze a hétköznapi szórakozottsághoz (amiről a mindennapi életben néha beszélünk - „Teljesen szklerózisom van, Megint elfelejtettem mindent”).
A sclerosis multiplex tünetei változóak, és attól függenek, hogy mely idegek érintettek. Köztük bénulás, egyensúlyi problémák, kognitív károsodás, az érzékszervek működésének megváltozása (a betegek negyedében a betegség kialakulása látóideggyulladás miatti látásromlással kezdődik).
A sclerosis multiplex modern kezelése sok kívánnivalót hagy maga után.
Hatékony kezelés még nincs, főleg, hogy ennek a betegségnek az okai még mindig nem ismertek, csak a környezet lehetséges hatásáról és a genetikai hajlamról vannak adatok. A kezeléshez a fájdalomcsillapítást és az izomgörcsöket csökkentő tüneti terápia mellett gyulladáscsökkentő glükokortikoid készítményeket, valamint az immunrendszer "rossz" aktivitásának visszaszorítását célzó immunmodulátorokat és immunszuppresszánsokat alkalmaznak. Mindezek a gyógymódok lelassíthatják a betegség kialakulását és csökkenthetik az exacerbációk gyakoriságát, de nem gyógyítják meg teljesen a beteget. Nincsenek olyan gyógyszerek, amelyek helyrehoznák a már sérült mielint.
Azonban hamarosan megjelenhet egy ilyen gyógyszer, amely kifejezetten a mielin helyreállítását célozza, és nem csak a kóros folyamat lelassítását. A svájci Biogen cég, a sclerosis multiplex kezelésére szolgáló gyógyszerek legnagyobb gyártója, Anti-LINGO-1 munkanév alatti fejlesztése jelenleg 2. fázisú klinikai vizsgálatokon megy keresztül. A gyógyszer egy monoklonális antitest, amely specifikusan tud kötődni a LINGO-1 fehérjéhez, ami megakadályozza a mielinizációs folyamatot és az új axonok képződését. Ennek megfelelően, ha ezt a fehérjét "kikapcsolják", a mielin elkezd helyreállni.
Állatkísérletekben az új gyógyszer alkalmazása 90 százalékban remielinizációhoz vezetett. Az Anti-LINGO-1-et szedő szklerózis multiplexben szenvedő betegek látóideg-vezetése jelenleg javult. A betegeken végzett klinikai vizsgálatok teljes eredményeit azonban csak 2016-ra kapják meg.