Cilvēkiem un mugurkaulniekiem ir vienots strukturālais plāns, un tos attēlo centrālā daļa - smadzenes un muguras smadzenes, kā arī perifērā daļa - nervi, kas stiepjas no centrālajiem orgāniem, kas ir nervu šūnu procesi - neironi.
Neiroglija šūnu iezīmes
Kā jau teicām, dendrītu un aksonu mielīna apvalku veido īpašas struktūras, kurām raksturīga zema nātrija un kalcija jonu caurlaidības pakāpe, un tāpēc tām ir tikai miera potenciāls (tie nevar vadīt nervu impulsus un veikt elektriskās izolācijas funkcijas).
Šīs struktūras tiek sauktas. Tās ietver:
- oligodendrocīti;
- šķiedru astrocīti;
- ependimas šūnas;
- plazmas astrocīti.
Visi no tiem ir veidoti no embrija ārējā slāņa - ektodermas, un tiem ir kopīgs nosaukums - makroglija. Simpātisko, parasimpātisko un somatisko nervu glia pārstāv Švāna šūnas (neirolemmocīti).
Oligodendrocītu struktūra un funkcijas
Tās ir daļa no centrālās nervu sistēmas un ir makroglijas šūnas. Tā kā mielīns ir proteīna-lipīdu struktūra, tas palīdz palielināt ierosmes ātrumu. Pašas šūnas veido elektriski izolējošu nervu galu slāni galvas un muguras smadzenēs, kas veidojas jau intrauterīnās attīstības periodā. Viņu procesi iesaiņo neironus, kā arī dendrītus un aksonus ārējās plazmlemmas krokās. Izrādās, mielīns ir galvenais elektriski izolējošais materiāls, kas norobežo jaukto nervu nervu procesus.

un to īpašības
Perifērās sistēmas nervu mielīna apvalku veido neirolemmocīti (Švāna šūnas). To atšķirīgā iezīme ir tāda, ka tie spēj veidot tikai viena aksona aizsargapvalku un nevar veidot procesus, kā tas ir raksturīgs oligodendrocītiem.
Starp Schwann šūnām 1-2 mm attālumā ir apgabali, kuros nav mielīna, tā sauktie Ranvier mezgli. Caur tiem elektriskie impulsi tiek veikti spazmīgi aksonā.
Lemmocīti spēj labot nervu šķiedras, kā arī veic.Ģenētisku aberāciju rezultātā lemmocītu membrānas šūnās sākas nekontrolēta mitotiska dalīšanās un augšana, kā rezultātā dažādās ķermeņa daļās attīstās audzēji - švannomas (neirinomas). nervu sistēma.
Mikroglia loma mielīna struktūras iznīcināšanā
Mikroglijas ir makrofāgi, kas spēj fagocitozi un spēj atpazīt dažādas patogēnās daļiņas – antigēnus. Pateicoties membrānas receptoriem, šīs glia šūnas ražo fermentus – proteāzes, kā arī citokīnus, piemēram, interleikīnu 1. Tas ir iekaisuma procesa un imunitātes mediators.
Interleikīns var sabojāt mielīna apvalku, kura funkcija ir izolēt aksiālo cilindru un uzlabot nervu impulsa vadītspēju. Tā rezultātā nervs ir "kails", un ierosmes ātrums ir strauji samazināts.

Turklāt citokīni, aktivizējot receptorus, izraisa pārmērīgu kalcija jonu transportēšanu neirona ķermenī. Proteāzes un fosfolipāzes sāk noārdīt nervu šūnu organellus un procesus, kas noved pie apoptozes – šīs struktūras nāves.
Tas sabrūk, sadaloties daļiņās, kuras aprij makrofāgi. Šo parādību sauc par eksitotoksicitāti. Tas izraisa neironu un to galu deģenerāciju, izraisot tādas slimības kā Alcheimera un Parkinsona slimība.
Pulpas nervu šķiedras
Ja neironu - dendrītu un aksonu procesi ir pārklāti ar mielīna apvalku, tad tos sauc par mīkstumu un inervē skeleta muskuļus, nonākot perifērās nervu sistēmas somatiskajā sadaļā. Nemielinizētās šķiedras veido veģetatīvo nervu sistēmu un inervē iekšējos orgānus.

Pulpa procesiem ir lielāks diametrs nekā nemaļīgajiem, un tie veidojas šādi: aksoni saliec glia šūnu plazmas membrānu un veido lineārus mesaksonus. Tad tie pagarinās un Švāna šūnas atkārtoti aptin ap aksonu, veidojot koncentriskus slāņus. Lemmocīta citoplazma un kodols pārvietojas uz ārējā slāņa reģionu, ko sauc par neirilemmu vai Švāna membrānu.
Lemmocīta iekšējais slānis sastāv no slāņainā mezoksona un tiek saukts par mielīna apvalku. Tās biezums dažādās nerva daļās nav vienāds.
Kā salabot mielīna apvalku
Ņemot vērā mikrogliju lomu nervu demielinizācijas procesā, mēs atklājām, ka makrofāgu un neirotransmiteru (piemēram, interleikīnu) iedarbībā mielīns tiek iznīcināts, kas savukārt izraisa neironu uztura pasliktināšanos un transmisijas traucējumus. nervu impulsi gar aksoniem.
Šī patoloģija provocē neirodeģeneratīvu parādību rašanos: kognitīvo procesu, galvenokārt atmiņas un domāšanas, pasliktināšanos, ķermeņa kustību un smalko motoriku koordinācijas traucējumu parādīšanos.

Rezultātā iespējama pilnīga pacienta invaliditāte, kas rodas autoimūno slimību rezultātā. Tāpēc jautājums par to, kā atjaunot mielīnu, šobrīd ir īpaši aktuāls. Šīs metodes galvenokārt ietver sabalansētu olbaltumvielu un lipīdu diētu, pareizu dzīvesveidu un sliktu ieradumu neesamību. Smagos slimību gadījumos medikamentozo ārstēšanu izmanto, lai atjaunotu nobriedušu glia šūnu - oligodendrocītu skaitu.
Cilvēku un mugurkaulnieku nervu sistēmai ir vienots strukturālais plāns, un to pārstāv centrālā daļa – smadzenes un muguras smadzenes, kā arī perifērā daļa – no centrālajiem orgāniem atiet ar nerviem, kas ir nervu šūnu – neironu procesi.
To kombinācija veido nervu audus, kuru galvenās funkcijas ir uzbudināmība un vadītspēja. Šīs īpašības galvenokārt skaidrojamas ar neironu čaumalu un to procesu strukturālajām iezīmēm, kas sastāv no vielas, ko sauc par mielīnu. Šajā rakstā mēs apsvērsim šī savienojuma struktūru un funkcijas, kā arī uzzināsim iespējamos veidus, kā to atjaunot.
Kāpēc neirocīti un to procesi ir pārklāti ar mielīnu
Nav nejaušība, ka dendritiem un aksoniem ir aizsargslānis, kas sastāv no proteīna-lipīdu kompleksiem. Fakts ir tāds, ka pārkāpums ir biofizikāls process, kura pamatā ir vāji elektriskie impulsi. Ja caur vadu plūst elektriskā strāva, tad pēdējais jāpārklāj ar izolācijas materiālu, lai samazinātu elektrisko impulsu izkliedi un novērstu strāvas stipruma samazināšanos. Mielīna apvalks veic tādas pašas funkcijas nervu šķiedrās. Turklāt tas ir atbalsts un arī nodrošina šķiedras jaudu.
Mielīna ķīmiskais sastāvs
Tāpat kā lielākajai daļai šūnu membrānu, tai ir lipoproteīnu raksturs. Turklāt tauku saturs šeit ir ļoti augsts - līdz 75%, bet olbaltumvielas - līdz 25%. Mielīns satur arī nelielu daudzumu glikolipīdu un glikoproteīnu. Tās ķīmiskais sastāvs atšķiras mugurkaula un galvaskausa nervos.
Pirmajā ir augsts fosfolipīdu saturs - līdz 45%, bet pārējais attiecas uz holesterīnu un cerebrozīdiem. Demielinizācija (tas ir, mielīna aizstāšana ar citām vielām nervu procesos) noved pie tādām smagām autoimūnām slimībām kā, piemēram, multiplā skleroze.
No ķīmiskā viedokļa šis process izskatīsies šādi: nervu šķiedru mielīna apvalks maina savu struktūru, kas galvenokārt izpaužas kā lipīdu procentuālā samazināšanās attiecībā pret olbaltumvielām. Turklāt holesterīna daudzums samazinās un ūdens saturs palielinās. Un tas viss noved pie pakāpeniskas mielīna nomaiņas, kas satur oligodendrocītus vai Švāna šūnas, makrofāgus, astrocītus un starpšūnu šķidrumu. Šādu bioķīmisko izmaiņu rezultāts būs straujš aksonu spējas samazinājums vadīt ierosmi līdz pilnīgai nervu impulsu pārejas bloķēšanai.
Neiroglija šūnu iezīmes
Kā jau teicām, dendrītu un aksonu mielīna apvalku veido īpašas struktūras, kurām raksturīga zema nātrija un kalcija jonu caurlaidības pakāpe, un tāpēc tām ir tikai miera potenciāls (tās nevar vadīt nervu impulsus un veikt elektriskās izolācijas funkcijas). ). Šīs struktūras sauc par glia šūnām. Tie ietver:
- oligodendrocīti;
- šķiedru astrocīti;
- ependimālās šūnas;
- plazmas astrocīti.
Visi no tiem ir veidoti no embrija ārējā slāņa - ektodermas, un tiem ir kopīgs nosaukums - makroglija. Simpātisko un parasimpātisko somatisko nervu glia pārstāv Švāna šūnas (neirolemocīti).
Oligodendrocītu struktūra un funkcijas
Tās ir daļa no centrālās nervu sistēmas un ir makroglijas šūnas. Tā kā mielīns ir proteīna-lipīdu struktūra, tas palīdz palielināt ierosmes ātrumu. Pašas šūnas veido elektriski izolējošu nervu galu slāni galvas un muguras smadzenēs, kas veidojas jau intrauterīnās attīstības periodā. Viņu procesi iesaiņo neironus, kā arī dendrītus un aksonus ārējās plazmlemmas krokās. Izrādās, mielīns ir galvenais elektriski izolējošais materiāls, kas norobežo jaukto nervu nervu procesus.
Švana šūnas un to īpašības
Perifērās sistēmas nervu mielīna apvalku veido neirolemmocīti (Švāna šūnas). To atšķirīgā iezīme ir tāda, ka tie spēj veidot tikai viena aksona aizsargapvalku un nevar veidot procesus, kā tas ir raksturīgs oligodendrocītiem. Starp Schwann šūnām 1-2 mm attālumā ir apgabali, kuros nav mielīna, tā sauktie Ranvier mezgli. Aiz tā aksonā spastiski tiek veikti elektriskie impulsi. Lemmocīti spēj atjaunot nervu šķiedras, kā arī veic trofisko funkciju. Ģenētisko aberāciju rezultātā lemmocītu apvalka šūnās sākas nekontrolēta mitotiska dalīšanās un augšana, kā rezultātā dažādās nervu sistēmas daļās attīstās audzēji, švannomas (neirinomas).
Mikroglia loma mielīna struktūras iznīcināšanā
Mikroglijas ir makrofāgi, kas spēj fagocitozi un spēj atpazīt dažādas patogēnās daļiņas – antigēnus. Pateicoties membrānas receptoriem, šīs glia šūnas ražo fermentus – proteāzes, kā arī citokīnus, piemēram, interleikīnu 1. Tas ir iekaisuma procesa un imunitātes mediators. Interleikīns var sabojāt mielīna apvalku, kura funkcija ir izolēt aksiālo cilindru un uzlabot nervu impulsu vadīšanu. Rezultātā nervs tiek “atsegts”, un ierosmes vadīšanas ātrums ir strauji samazināts.
Turklāt citokīni, aktivizējot receptorus, izraisa pārmērīgu kalcija jonu transportēšanu neirona ķermenī. Proteāzes un fosfolipāzes sāk noārdīt nervu šūnu organellus un procesus, kas noved pie apoptozes – šīs struktūras nāves. Tas sabrūk, sadaloties daļiņās, kuras aprij makrofāgi. Šo parādību sauc par eksitotoksicitāti. Tas izraisa neironu un to galu deģenerāciju, izraisot tādas slimības kā Alcheimera un Parkinsona slimība.
Pulpas nervu šķiedras
Ja neironu - dendrītu un aksonu procesi ir pārklāti ar mielīna apvalku, tad tos sauc par mīkstumu un inervē skeleta muskuļus, nonākot perifērās nervu sistēmas somatiskajā sadaļā. Nemielinizētās šķiedras veido veģetatīvo nervu sistēmu un inervē iekšējos orgānus.
Pulpveida procesiem ir lielāks diametrs nekā neplaušu procesiem, un tie veidojas šādi: aksoni saliec glia šūnu plazmas membrānu un veido lineārus mesaksonus. Pēc tam tās palielinās, un Švāna šūnas atkārtoti aptin ap aksonu, veidojot koncentriskus slāņus. Lemmocīta citoplazma un kodols pārvietojas uz ārējā slāņa reģionu, ko sauc par neirilemmu vai Švāna membrānu. Lemmocīta iekšējais slānis sastāv no slāņainā mezoksona un tiek saukts par mielīna apvalku. Tās biezums dažādās nerva daļās nav vienāds.
Kā salabot mielīna apvalku
Ņemot vērā mikrogliju lomu nervu demielinizācijas procesā, mēs atklājām, ka makrofāgu un neirotransmiteru (piemēram, interleikīnu) iedarbībā mielīns tiek iznīcināts, kas savukārt noved pie neironu uztura pasliktināšanās un transmisijas pārkāpuma. nervu impulsi gar aksoniem. Šī patoloģija provocē neirodeģeneratīvu parādību rašanos: kognitīvo procesu, galvenokārt atmiņas un domāšanas, pasliktināšanos, ķermeņa kustību un smalko motoriku koordinācijas traucējumu parādīšanos.
Rezultātā iespējama pilnīga pacienta invaliditāte, kas rodas autoimūno slimību rezultātā. Tāpēc jautājums par to, kā atjaunot mielīnu, šobrīd ir īpaši aktuāls. Šīs metodes, pirmkārt, ietver sabalansētu olbaltumvielu un lipīdu diētu, pareizu dzīvesveidu un sliktu ieradumu neesamību. Smagos slimību gadījumos medikamentozo ārstēšanu izmanto, lai atjaunotu nobriedušu glia šūnu - oligodendrocītu skaitu.
Publicēšanas datums: 26.05.17Centrālā nervu sistēma (CNS) ir vienots mehānisms, kas atbild par apkārtējās pasaules uztveri un refleksiem, kā arī par iekšējo orgānu un audu sistēmas kontroli. Pēdējo punktu veic centrālās nervu sistēmas perifērā daļa ar īpašu šūnu palīdzību, ko sauc par neironiem. No tiem sastāv nervu audi, kas kalpo impulsu pārraidīšanai.
Procesus, kas nāk no neirona ķermeņa, ieskauj aizsargslānis, kas baro nervu šķiedras un paātrina impulsu pārnešanu, un šādu aizsardzību sauc par mielīna apvalku. Jebkurš signāls, kas tiek pārraidīts caur nervu šķiedrām, atgādina strāvas izlādi, un tas ir to ārējais slānis, kas neļauj tā stiprumam samazināties.
Ja mielīna apvalks ir bojāts, tad pilnīga uztvere šajā ķermeņa daļā tiek zaudēta, bet šūna var izdzīvot un bojājumi ar laiku sadzīst. Pie pietiekami nopietniem ievainojumiem būs nepieciešamas zāles, kas paredzētas nervu šķiedru atjaunošanai, piemēram, Milgamma, Copaxone un citi. Pretējā gadījumā nervs galu galā nomirs un uztvere samazināsies. Pie slimībām, kurām raksturīga šī problēma, pieder radikulopātija, polineiropātija u.c., taču par bīstamāko patoloģisko procesu ārsti uzskata multiplo sklerozi (MS). Neskatoties uz dīvaino nosaukumu, slimībai nav nekāda sakara ar šo vārdu tiešu definīciju un tulkojumā nozīmē "vairākas rētas". Tie rodas uz mielīna apvalka muguras smadzenēs un smadzenēs imūnsistēmas mazspējas dēļ, tāpēc MS ir autoimūna slimība. Nervu šķiedru vietā fokusa vietā parādās rēta, kas sastāv no saistaudiem, caur kuriem impulss vairs nevar pareizi iziet.
Vai ir iespējams kaut kā atjaunot bojātos nervu audus vai arī tie uz visiem laikiem paliks kroplā stāvoklī? Ārsti joprojām nevar precīzi atbildēt un vēl nav nākuši klajā ar pilnvērtīgu medikamentu, lai atjaunotu jutību pret nervu galiem. Tā vietā ir dažādi medikamenti, kas var samazināt demielinizācijas procesu, uzlabot bojāto vietu uzturu un aktivizēt mielīna apvalka atjaunošanos.
Milgamma ir neiroprotektors vielmaiņas atjaunošanai šūnās, kas ļauj palēnināt mielīna iznīcināšanas procesu un uzsākt tā atjaunošanos. Zāļu pamatā ir B grupas vitamīni, proti:
- Tiamīns (B1). Tas ir nepieciešams cukura uzsūkšanai organismā un enerģijai. Ar akūtu tiamīna deficītu cilvēkam tiek traucēts miegs un pasliktinās atmiņa. Viņš kļūst nervozs un dažreiz nomākts, kā depresijā. Dažos gadījumos ir parestēzijas simptomi (zosāda, samazināta jutība un tirpšana pirkstu galos);
- Piridoksīns (B6). Šim vitamīnam ir svarīga loma aminoskābju, kā arī dažu hormonu (dopamīna, serotonīna u.c.) ražošanā. Neskatoties uz retiem piridoksīna trūkuma gadījumiem organismā, tā deficīta dēļ ir iespējama garīgo spēju samazināšanās un imūnās aizsardzības pavājināšanās;
- Ciānkobalamīns (B12). Tas kalpo, lai uzlabotu nervu šķiedru vadītspēju, kā rezultātā uzlabojas jutība, kā arī uzlabo asins sintēzi. Ar cianokobalamīna trūkumu cilvēkam attīstās halucinācijas, demence (demence), rodas sirds ritma traucējumi un parestēzija.
Pateicoties šim sastāvam, Milgama spēj apturēt šūnu oksidēšanos ar brīvajiem radikāļiem (reaktīvām vielām), kas ietekmēs audu un nervu galu jutīguma atjaunošanos. Pēc tablešu lietošanas kursa simptomi samazinās un vispārējais stāvoklis uzlabojas, un zāles jālieto 2 posmos. Pirmajā gadījumā jums būs jāveic vismaz 10 injekcijas, pēc tam jāpāriet uz tabletēm (Milgamma compositum) un jālieto tās 3 reizes dienā 1,5 mēnešus.

Stafaglabrīna sulfātu jau ilgu laiku izmanto, lai atjaunotu audu un pašu nervu šķiedru jutīgumu. Augs, no kura saknēm iegūtas šīs zāles, aug tikai subtropu un tropu klimatā, piemēram, Japānā, Indijā un Birmā, un to sauc par Stefānijas gludo. Ir gadījumi, kad laboratorijā tiek iegūts stafaglabrīna sulfāts. Varbūt tas ir saistīts ar faktu, ka stephania smooth var audzēt kā suspensijas kultūru, tas ir, suspendētā stāvoklī stikla kolbās ar šķidrumu. Pati par sevi zāles ir sulfāta sāls, kam ir augsta kušanas temperatūra (vairāk nekā 240 ° C). Tas attiecas uz alkaloīdu (slāpekli saturošu savienojumu) stefarīnu, kas tiek uzskatīts par proaporfīna pamatu.
Stefaglabrīna sulfāts kalpo, lai samazinātu hidrolāžu (holīnesterāzes) klases enzīmu aktivitāti un uzlabotu gludo muskuļu tonusu, kas atrodas asinsvadu sieniņās, orgānos (iekšpusē dobumā) un limfmezglos. Ir arī zināms, ka zāles ir nedaudz toksiskas un var pazemināt asinsspiedienu. Vecajās dienās zāles lietoja kā antiholīnesterāzes līdzekli, bet tad zinātnieki nonāca pie secinājuma, ka stefaglabrīna sulfāts ir saistaudu augšanas aktivitātes inhibitors. No tā izrādās, ka tas aizkavē tā attīstību un uz nervu šķiedrām neveidojas rētas. Tāpēc zāles sāka aktīvi lietot PNS bojājumiem.
Pētījuma laikā eksperti varēja redzēt Schwann šūnu augšanu, kas ražo mielīnu perifērajā nervu sistēmā. Šī parādība nozīmē, ka zāļu ietekmē pacients ievērojami uzlabo impulsa vadīšanu gar aksonu, jo ap to atkal sāka veidoties mielīna apvalks. Kopš rezultātu iegūšanas zāles ir kļuvušas par cerību daudziem cilvēkiem, kuriem diagnosticētas neārstējamas demielinizējošas patoloģijas.

Autoimūnās patoloģijas problēmu nebūs iespējams atrisināt tikai ar nervu šķiedru atjaunošanu. Patiešām, neatkarīgi no tā, cik bojājumu perēkļu ir jānovērš, problēma atgriezīsies, jo imūnsistēma reaģē uz mielīnu kā svešķermeni un iznīcina to. Līdz šim šādu patoloģisku procesu nav iespējams novērst, taču vairs nevar brīnīties, vai nervu šķiedras ir atjaunotas vai nē. Cilvēkiem ir jāturpina saglabāt savu stāvokli, nomācot imūnsistēmu un lietojot tādas zāles kā stefaglabrīna sulfāts, lai saglabātu savu veselību.
Zāles var lietot tikai parenterāli, tas ir, caur zarnām, piemēram, injekcijas veidā. Deva šajā gadījumā nedrīkst pārsniegt 7-8 ml 0,25% šķīduma dienā 2 injekcijām. Spriežot pēc laika, mielīna apvalks un nervu gali parasti kaut kādā mērā tiek atjaunoti pēc 20 dienām, un tad ir nepieciešams pārtraukums un var saprast, cik ilgi tas turpināsies, uzzinot par to no ārsta. Labāko rezultātu, pēc ārstu domām, var sasniegt uz mazu devu rēķina, jo blakusparādības attīstās daudz retāk un palielinās ārstēšanas efektivitāte.
Laboratorijas apstākļos, veicot eksperimentus ar žurkām, tika konstatēts, ka ar zāļu Stefaglabrin sulfate koncentrāciju 0,1-1 mg / kg ārstēšana ir ātrāka nekā bez tā. Terapijas kurss beidzās agrāk, salīdzinot ar dzīvniekiem, kuri šīs zāles nelietoja. Pēc 2-3 mēnešiem grauzēju nervu šķiedras tika gandrīz pilnībā atjaunotas, un impulss tika pārraidīts pa nervu bez kavēšanās. Eksperimenta subjektiem, kuri tika ārstēti bez šīs zāles, atveseļošanās ilga apmēram sešus mēnešus, un ne visi nervu gali atgriezās normālā stāvoklī.
Copaxone

Nav iespējams izārstēt multiplo sklerozi, taču ir zāles, kas var samazināt imūnsistēmas ietekmi uz mielīna apvalku, un Copaxone ir viena no tām. Autoimūno slimību būtība ir tāda, ka imūnsistēma iznīcina mielīnu, kas atrodas uz nervu šķiedrām. Sakarā ar to pasliktinās impulsu vadītspēja, un Copaxone spēj mainīt ķermeņa aizsardzības sistēmas mērķi uz sevi. Nervu šķiedras paliek neskartas, bet, ja ķermeņa šūnas jau ir pārņēmušas mielīna apvalka eroziju, tad zāles spēs tās atgrūst. Šī parādība rodas tāpēc, ka zāles pēc struktūras ir ļoti līdzīgas mielīnam, tāpēc imūnsistēma pārvērš uzmanību uz to.
Zāles spēj ne tikai uzņemties ķermeņa aizsardzības sistēmas uzbrukumu, bet arī ražo īpašas imūnsistēmas šūnas, lai samazinātu slimības intensitāti, ko sauc par Th2-limfocītiem. To ietekmes un veidošanās mehānisms vēl nav pienācīgi izpētīts, taču ir dažādas teorijas. Ekspertu vidū ir viedoklis, ka Th2-limfocītu sintēzē ir iesaistītas epidermas dendrītiskās šūnas.
Izstrādātie supresori (mutētie) limfocīti, nokļūstot asinīs, ātri iekļūst tajā nervu sistēmas daļā, kur atrodas iekaisuma perēklis. Šeit Th2 limfocīti mielīna ietekmes dēļ ražo citokīnus, tas ir, pretiekaisuma molekulas. Tie sāk pakāpeniski mazināt iekaisumu šajā smadzeņu daļā, tādējādi uzlabojot nervu galu jutīgumu.
Zāļu ieguvums ir ne tikai pašas slimības ārstēšanai, bet arī pašām nervu šūnām, jo Copaxone ir neiroprotektors. Aizsardzības efekts izpaužas smadzeņu šūnu augšanas stimulācijā un lipīdu metabolisma uzlabošanā. Mielīna apvalks galvenokārt sastāv no lipīdiem, un daudzos patoloģiskos procesos, kas saistīti ar nervu šķiedru bojājumiem, notiek to oksidēšanās, tāpēc mielīns tiek bojāts. Zāles Copaxone spēj novērst šo problēmu, jo tas palielina ķermeņa dabisko antioksidantu (urīnskābes). Sakarā ar to, kā paaugstinās urīnskābes līmenis, nav zināms, taču šis fakts ir pierādīts daudzu eksperimentu gaitā.
Zāles kalpo, lai aizsargātu nervu šūnas un samazinātu paasinājumu smagumu un biežumu. To var kombinēt ar zālēm Stefaglabrin sulfate un Milgamma.
Mielīna apvalks sāks atgūties, jo palielinās Schwann šūnu augšana, un Milgamma uzlabos intracelulāro metabolismu un pastiprinās abu zāļu iedarbību. Ir stingri aizliegts tos lietot atsevišķi vai mainīt devu atsevišķi.
Vai ir iespējams atjaunot nervu šūnas un cik ilgi tas prasīs, var atbildēt tikai speciālists, koncentrējoties uz izmeklēšanas rezultātiem. Ir aizliegts patstāvīgi lietot jebkādas zāles, lai uzlabotu audu jutīgumu, jo lielākajai daļai no tām ir hormonāls pamats, kas nozīmē, ka organisms tās ir grūti panesamas.
NERVU ŠĶIEDRAS
Nervu šķiedras ir neironu procesi, kas pārklāti ar glia apvalkiem. Ir divu veidu nervu šķiedras - nemielinētas un mielinētas. Abi veidi sastāv no centrāli guļoša neirona procesa (aksiālā cilindra), ko ieskauj oligodendroglia šūnu apvalks (PNS tos sauc par lemmocītiem vai Švana šūnām).
nemielinizētas nervu šķiedras pieaugušam cilvēkam tie atrodas galvenokārt veģetatīvā nervu sistēmā un tiem raksturīgs salīdzinoši zems nervu impulsu vadīšanas ātrums (0.5-2 jaunkundze). Tie veidojas, iegremdējot aksiālo cilindru (aksonu) lemmocītu citoplazmā, kas atrodas dzīslu veidā. Šajā gadījumā lemmocīta plazmolemma saliecas, apņemot aksonu, un veido dublēšanos - mesaksonu (att. 14-7). Bieži viena lemmocīta citoplazmā var būt līdz 10-20 asu cilindri. Šāda šķiedra atgādina elektrisko kabeli un tāpēc to sauc par kabeļa tipa šķiedru. Šķiedras virsma ir pārklāta ar bazālo membrānu. CNS, īpaši tās attīstības gaitā, ir aprakstītas nemielinizētas šķiedras, kas sastāv no "kaila" aksona, bez lemmocītu apvalka.
Rīsi. 14-7. Mielinētu (1-3) un nemielinētu (4) nervu šķiedru veidošanās perifērajā nervu sistēmā. Nervu šķiedra veidojas, iegremdējot nervu šūnas aksonu (A) lemmocīta (LC) citoplazmā. Kad veidojas mielīna šķiedra, ap A tiek apvilkta LC plazmolemmas dublēšanās - mesaksons (MA), veidojot mielīna apvalka (MO) pagriezienus. Attēlā redzamajā bez mielīna šķiedras LC (kabeļa tipa šķiedras) citoplazmā ir iegremdēti vairāki A. Es esmu LC kodols.

mielinētas nervu šķiedras atrodami CNS un PNS, un tiem raksturīgs liels nervu impulsu vadīšanas ātrums (5-120 jaunkundze). Mielinizētās šķiedras parasti ir biezākas nekā nemielinizētās šķiedras, un tajās ir lielāka diametra aksiālie cilindri. Mielīna šķiedrā aksiālo cilindru tieši ieskauj īpašs mielīna apvalks, ap kuru ir plāns slānis, kas ietver citoplazmu un lemmocīta kodolu - neirolemmu (att. 14-8 un 14-9). Ārpusē šķiedra ir arī pārklāta ar bazālo membrānu. Mielīna apvalks satur augstu lipīdu koncentrāciju un ir intensīvi krāsots ar osmīnskābi, kas gaismas mikroskopā izskatās kā viendabīgs slānis, bet elektronu mikroskopā tiek konstatēts, ka tas rodas, saplūstot daudzām (līdz 300) membrānas spoles (plāksnes).
Rīsi. 14-8. Mielinizētās nervu šķiedras struktūra. Mielīna šķiedra sastāv no aksiāla cilindra jeb aksona (A), ko tieši ieskauj mielīna apvalks (MO) un neirolemma (NL), ieskaitot citoplazmu (CL) un lemmocītu kodolu (NL). Ārpusē šķiedra ir pārklāta ar bazālo membrānu (BM). MO apgabaliem, kuros ir saglabātas spraugas starp mielīna pagriezieniem, kas ir piepildītas ar CL un tāpēc nav iekrāsotas ar osmiju, ir mielīna iegriezumu (MN) forma.
Mielīna apvalka veidošanās rodas aksiālā cilindra un oligodendroglia šūnu mijiedarbības laikā ar dažām atšķirībām PNS un CNS.
Mielīna apvalka veidošanās PNS : aksiālā cilindra iegremdēšanu lemocītā pavada gara mezaksona veidošanās, kas sāk griezties ap aksonu, veidojot pirmos brīvi sakārtotos mielīna apvalka pagriezienus (sk. 14-7). Palielinoties apgriezienu (plāksnīšu) skaitam mielīna nobriešanas procesā, tie tiek sakārtoti arvien blīvāk un daļēji saplūst; spraugas starp tām, kas piepildītas ar lemmocīta citoplazmu, tiek saglabātas tikai atsevišķās vietās, kas nav iekrāsotas ar osmija - mielīna iecirtumiem (Šmits-Lantermans). Mielīna apvalka veidošanās laikā lemmocīta citoplazma un kodols tiek nospiesti uz šķiedras perifēriju, veidojot neirolemmu. Mielīna apvalkam ir pārtraukta gaita visā šķiedras garumā.

Rīsi. 14-9. Mielinizētās nervu šķiedras ultrastrukturālā organizācija. Ap aksonu (A) atrodas mielīna apvalka (MMO) spoles, kas ārēji pārklātas ar neirolemmu un ietver citoplazmu (CL) un lemmocīta kodolu (NL). Šķiedru no ārpuses ieskauj bazālā membrāna (BM). CL papildus neirolemmai veido iekšējo loksni (IL), kas atrodas tieši blakus A (atrodas starp to un SMO), tā atrodas arī zonā, kas atbilst blakus esošo lemmocītu robežai - mezgla pārtveršanai (NC), kur nav mielīna apvalka, un vietās ar vaļēju WMO sakraušanu - mielīna iegriezumi (MN).
Mezglu pārtveršana (Ranvier)- apgabali blakus esošo lemmocītu robežas apvidū, kuros nav mielīna apvalka, un aksonu klāj tikai blakus esošo lemmocītu savstarpējās digitācijas procesi (sk. 14.-9. att.). Mezglu pārtveršana atkārtojas visā mielīna šķiedras gaitā ar intervālu, kas vidēji vienāds ar 1-2 mm. Mezgla mezgla reģionā aksons bieži paplašinās, un tā plazmolemmā ir daudz nātrija kanālu (kuru nav ārpus mezgliem zem mielīna apvalka).
Depolarizācijas izplatīšanās mielīna šķiedrās veic lēcienos no pārtveršanas līdz pārtveršanai (sāļš). Depolarizāciju viena mezgla savienojuma reģionā pavada tās strauja pasīvā izplatīšanās pa aksonu līdz nākamajam krustojumam (jo strāvas noplūde starpmezglu reģionā ir minimāla mielīna augsto izolācijas īpašību dēļ). Nākamā krustojuma zonā impulss liek ieslēgties esošajiem jonu kanāliem un parādās jauns lokālās depolarizācijas apgabals utt.
Mielīna apvalka veidošanās CNS: aksiālais cilindrs neiegrimst oligodendrocīta citoplazmā, bet tiek pārklāts ar tā plakano procesu, kas pēc tam griežas ap to, zaudējot citoplazmu, un tā spoles pārvēršas mielīna apvalka plāksnēs.

elkoņi (14.-10. att.). Atšķirībā no Švana šūnām viens CNS oligodendrocīts ar saviem procesiem var piedalīties daudzu (līdz 40-50) nervu šķiedru mielinizēšanā. Aksonu vietas Ranvier mezglu zonā CNS nesedz oligodendrocītu citoplazma.
Rīsi. 14-10. Mielīna šķiedru veidošanās ar oligodendrocītiem CNS. 1 - neirona aksonu (A) pārklāj oligodendrocīta (ODC) plakans process (PO), kura spoles pārvēršas mielīna apvalka (MO) plāksnēs. 2 - viens ODC ar saviem procesiem var piedalīties daudzu A mielinizācijā. A zonas mezglu pārtveršanas zonā (NC) nav pārklātas ar ODC citoplazmu.
Veidotā mielīna veidošanās un bojājuma pārkāpums pamatā ir vairākas nopietnas nervu sistēmas slimības. Mielīns CNS var būt autoimūno bojājumu mērķis T-limfocīti un makrofāgi ar tās iznīcināšanu (demielinizāciju). Šis process aktīvi norisinās multiplās sklerozes gadījumā, kas ir nopietna neskaidra (iespējams, vīrusu) slimība, kas saistīta ar dažādu funkciju traucējumiem, paralīzes attīstību un jutīguma zudumu. Neiroloģisko traucējumu raksturu nosaka bojāto zonu topogrāfija un lielums. Ar dažiem vielmaiņas traucējumiem ir mielīna veidošanās traucējumi - leikodistrofija, kas bērnībā izpaužas ar smagiem nervu sistēmas bojājumiem.
Nervu šķiedru klasifikācija
Nervu šķiedru klasifikācija balstās uz atšķirībām to struktūrā un funkcijās (nervu impulsu ātrumā). Ir trīs galvenie nervu šķiedru veidi:
1. A tipa šķiedras - biezs, mielinēts, ar tālu attāliem mezglu pārtvērumiem. Vadīt impulsus lielā ātrumā
(15-120 m/s); iedalīts 4 apakštipos (α, β, γ, δ) ar samazinātu diametru un impulsa vadīšanas ātrumu.
2. B tipa šķiedras - vidēja biezuma, mielīna, mazāks diametrs,
nekā A tipa šķiedrām, ar plānāku mielīna apvalku un mazāku nervu impulsu vadīšanas ātrumu (5-15 m/s).
3. C tipa šķiedras - plānas, nemielinizētas, vadīt impulsus ar salīdzinoši mazu ātrumu(0,5-2 m/s).
Nervu šķiedru reģenerācija PNS ietver dabiski izvērstu sarežģītu procesu secību, kuras laikā neironu process aktīvi mijiedarbojas ar glia šūnām. Faktiskā šķiedru reģenerācija notiek pēc virknes reaktīvu izmaiņu, ko izraisa to bojājumi.
Reaktīvās izmaiņas nervu šķiedrā pēc tās pārgriešanas. 1.nedēļā pēc nervu šķiedras griešanas attīstās aksona proksimālās (vistuvāk neirona ķermenim) daļas augšupejoša deģenerācija, kuras beigās veidojas pagarinājums (retrakcijas kolba). Mielīna apvalks bojājuma zonā sairst, neirona ķermenis uzbriest, kodols nobīdās uz perifēriju, izšķīst hromatofīlā viela (14.-11.att.).
Šķiedras distālajā daļā pēc tās šķērsgriezuma tiek novērota lejupejoša deģenerācija ar pilnīgu aksona iznīcināšanu, mielīna sadalīšanos un sekojošu detrīta fagocitozi ar makrofāgiem un glia.
Strukturālās transformācijas nervu šķiedras reģenerācijas laikā. Pēc 4-6 nedēļām. atjaunojas neirona struktūra un funkcija, no retrakcijas kolbas sāk augt plāni zari (augšanas konusi) šķiedras distālās daļas virzienā. Schwann šūnas šķiedras proksimālajā daļā proliferējas, veidojot lentes (Büngner) paralēli šķiedras gaitai. Šķiedras distālajā daļā Švāna šūnas arī saglabājas un mitotiski dalās, veidojot lentes, kas savienojas ar līdzīgiem veidojumiem proksimālajā daļā.
Reģenerējošais aksons aug distālajā virzienā ar ātrumu 3-4 mm/dienā. pa Büngner lentēm, kurām ir atbalsta un vadošā loma; Schwann šūnas veido jaunu mielīna apvalku. Nodrošinājums un aksonu termināli tiek atjaunoti dažu mēnešu laikā.

Rīsi. 14-11. Mielinizētās nervu šķiedras reģenerācija (pēc R.Krstiča, 1985, ar izmaiņām). 1 - pēc nervu šķiedras pārgriešanas aksona (A) proksimālajā daļā notiek augšupejoša deģenerācija, mielīna apvalks (MO) bojājuma zonā sadalās, neirona perikarions (PC) uzbriest, kodols nobīdās. uz perifēriju, hromatofilā viela (CS) sadalās (2). Distālā daļa, kas saistīta ar inervēto orgānu (dotajā piemērā skeleta muskuļi), tiek pakļauta lejupvērsta deģenerācijai ar pilnīgu A iznīcināšanu, MO sadalīšanos un detrīta fagocitozi, ko veic makrofāgi (MF) un glia. Lemmocīti (LC) saglabājas un mitotiski sadalās, veidojot pavedienus - Bīgnera lentes (LB), savienojoties ar līdzīgiem veidojumiem šķiedras proksimālajā daļā (plānās bultiņas). Pēc 4-6 nedēļām tiek atjaunota neirona struktūra un funkcija, no proksimālās daļas A distāli izaug plāni zari (treknā bultiņa), augot gar LB (3). Nervu šķiedras reģenerācijas rezultātā tiek atjaunota saikne ar mērķa orgānu (muskuli) un tā atrofija, ko izraisa traucēta inervācija, regresē (4). Ja rodas šķērslis (P) atjaunošanās A ceļā (piemēram, saistaudu rēta), nervu šķiedras sastāvdaļas
veido traumatisku neiromu (TN), kas sastāv no augošiem A un LC zariem (5).
reģenerācijas apstākļi ir: nav bojājumu neirona ķermenim, neliels attālums starp nervu šķiedras daļām, nav saistaudu, kas var aizpildīt plaisu starp šķiedras daļām. Kad reģenerējošā aksona ceļā rodas obstrukcija, veidojas traumatiska (amputācijas) neiroma, kas sastāv no augoša aksona un Švāna šūnām, kas pielodētas saistaudos.
CNS nenotiek nervu šķiedru atjaunošanās : lai gan CNS neironiem ir iespēja atjaunot savus procesus, tas nenotiek, acīmredzot mikrovides nelabvēlīgās ietekmes dēļ. Pēc neirona bojājumiem mikroglijas, astrocīti un hematogēnie makrofāgi fagocitizē detrītu iznīcinātās šķiedras zonā, un proliferējošie astrocīti veido blīvu glia rētu tās vietā.
NERVU BEIGAS
Nervu galiem- nervu šķiedru gala ierīces. Atbilstoši to funkcijām tos iedala trīs grupās:
1) starpneironālie kontakti (sinapses)- nodrošināt funkcionālu savienojumu starp neironiem;
2) eferentās (efektor) galotnes- pārraida signālus no nervu sistēmas uz izpildorgāniem (muskuļiem, dziedzeriem), atrodas uz aksoniem;
3) receptoru (jutīgās) galotnesuztver kairinājumus no ārējās un iekšējās vides, atrodas uz dendritiem.
STARPEIRONU KONTAKTI (SINAPSE)
Starpneironālie kontakti (sinapses) sadalīts elektriskajā un ķīmiskajā.
elektriskās sinapses reti sastopams zīdītāju CNS; tiem ir spraugu savienojumu struktūra, kurā sinaptiski savienoto šūnu (pre- un postsinaptisko) membrānas ir atdalītas ar 2 nm platu spraugu, ko caurdur konnekoni. Pēdējās ir caurules, ko veido olbaltumvielu molekulas, un tās kalpo kā ūdens kanāli, pa kuriem mazās molekulas un jonus var transportēt no vienas šūnas uz otru.

citu (skat. 3. nodaļu). Kad darbības potenciāls, kas izplatās pāri vienas šūnas membrānai, sasniedz spraugas savienojumu, elektriskā strāva pasīvi plūst caur spraugu no vienas šūnas uz otru. Impulsu var pārraidīt abos virzienos un praktiski bez kavēšanās.
Ķīmiskās sinapses- visizplatītākais veids zīdītājiem. To darbības pamatā ir elektriskā signāla pārvēršana ķīmiskā signālā, kas pēc tam tiek pārveidots atpakaļ elektriskajā signālā. Ķīmiskā sinapse sastāv no trim sastāvdaļām: presinaptiskās daļas, postsinaptiskās daļas un sinaptiskās plaisas (14.-12. att.). Presinaptiskā daļa satur (neiro)raidītāju, kas nervu impulsa ietekmē tiek izlaists sinaptiskajā spraugā un, saistoties ar postsinaptiskās daļas receptoriem, izraisa izmaiņas tās membrānas jonu caurlaidībā, kas noved pie tās. depolarizācija (uzbudināmās sinapsēs) vai hiperpolarizācija (inhibējošās sinapsēs). Ķīmiskās sinapses atšķiras no elektriskām sinapsēm ar vienpusēju impulsu vadīšanu, to pārraides aizkavēšanos (sinaptiskā aizkave 0,2–0,5 ms) un postsinaptiskā neirona ierosināšanu un inhibīciju.
Rīsi. 14-12. Ķīmiskās sinapses struktūra. Presinaptiskajai daļai (PRSP) ir termināla pogas (CB) forma, un tajā ietilpst: sinaptiskie pūslīši (SP), mitohondriji (MTX), neirotubuli (NT), neirofilamenti (NF), presinaptiskā membrāna (PRSM) ar presinaptisko blīvējumu (PRSU). ). Postsinaptiskā daļa (PSCH) ietver postsinaptisko membrānu (POSM) ar postsinaptisko blīvējumu (POSU). Sinaptiskā plaisa (SC) satur intrasinaptiskos pavedienus (ISF).
1. presinaptiskā daļa veido aksons tā gaitā (iet sinapsei) vai ir aksona pagarināta gala daļa (gala pumpurs). Tajā ir mitohondriji, aER, neirofilamenti, neirotubulas un sinaptiskās pūslīši ar diametru 20-65 nm, kas satur neirotransmiteru. Pūšļu satura forma un raksturs ir atkarīgs no tajos esošajiem neirotransmiteriem. Apaļi gaiši pūslīši parasti satur acetilholīnu, pūslīši ar kompaktu blīvu centru – norepinefrīnu, lielas blīvas pūslīši ar vieglu zemmembrānas malu – peptīdus. Neirotransmiteri tiek ražoti neirona ķermenī un ar ātrās transportēšanas mehānismu tiek transportēti uz aksonu galiem, kur tie tiek nogulsnēti. Daļēji sinaptiskās pūslīši veidojas pašā sinapsē, atdaloties no AER cisternām. Plazmolemmas iekšējā pusē, kas vērsta pret sinaptisko spraugu (presinaptisko membrānu), ir presinaptisks blīvējums, ko veido fibrilāra sešstūra proteīna tīkls, kura šūnas veicina vienmērīgu sinaptisko pūslīšu sadalījumu pa membrānas virsmu.
2. postsinaptiskā daļa To attēlo postsinaptiskā membrāna, kas satur īpašus integrālo proteīnu kompleksus - sinaptiskos receptorus, kas saistās ar neiromediatoru. Membrāna ir sabiezējusi, jo zem tās uzkrājas blīvs pavedienveida proteīna materiāls (postsinaptiskā sablīvēšanās). Atkarībā no tā, vai starpneironu sinapses postsinaptiskā daļa ir dendrīts, neirona ķermenis vai (retāk) tā aksons, sinapses tiek iedalītas attiecīgi aksodendrītiskajās, aksosomatiskajās un aksoaksonālajās.
3. sinaptiskā plaisa 20-30 nm platumā dažkārt ir 5 nm biezi šķērseniski glikoproteīna intrasinaptiskie pavedieni, kas ir specializēta glikokaliksa elementi, kas nodrošina pre- un postsinātiskās daļas adhezīvās saites, kā arī virzīta mediatora difūzija.
Nervu impulsa pārnešanas mehānisms ķīmiskajā sinapsē. Nervu impulsa ietekmē tiek aktivizēti no sprieguma atkarīgie presinaptiskās membrānas kalcija kanāli; Sa 2+ steidzas uz aksonu, sinaptisko pūslīšu membrānas Ca2+ klātbūtnē saplūst ar presinaptisko membrānu, un to saturs (mediators) ar eksocitozes mehānisma palīdzību tiek izvadīts sinaptiskajā spraugā. Iedarbojoties uz postsinaptiskās membrānas receptoriem, mediators izraisa vai nu tā depolarizāciju, postsinaptiskā darbības potenciāla rašanos un nervu impulsa veidošanos, vai arī tā hiperpigmentāciju.
polarizācija, izraisot inhibējošu reakciju. Uzbudinošie mediatori, piemēram, ir acetilholīns un glutamāts, savukārt inhibīciju veic GABA un glicīns.
Pēc mediatora mijiedarbības ar postsinaptiskās membrānas receptoriem pārtraukšanas lielāko daļu endocitozes uztver presinaptiskā daļa, mazāko daļu izkliedē telpā un uztver apkārtējās glia šūnas. Dažus mediatorus (piemēram, acetilholīnu) fermenti sadala komponentos, kurus pēc tam uztver presinaptiskā daļa. Sinaptiskās pūslīšu membrānas, kas iestrādātas presinaptiskajā membrānā, tiek tālāk iekļautas endocītu izklātajās vezikulās un atkārtoti izmantotas, lai veidotu jaunas sinaptiskās pūslīšus.
Ja nav nervu impulsa, presinaptiskā daļa atbrīvo atsevišķas nelielas mediatora daļas, izraisot spontānus miniatūras potenciālus postsinaptiskajā membrānā.
EFERENTĀS (EFEKTORS) NERVU GALAS
Eferenti (efektoru) nervu gali Atkarībā no inervētā orgāna rakstura tos iedala motoros un sekrēcijas. Motora galos atrodami šķērssvītrotajos un gludajos muskuļos, sekrēcijas – dziedzeros.
Neiromuskulārais gals (neiromuskulārais savienojums, motora plāksne) - motorā neirona aksona motorais gals uz šķērssvītroto somatisko muskuļu šķiedrām - sastāv no aksona gala atzarojuma, kas veido presinaptisko daļu, specializētas zonas uz muskuļu šķiedras, kas atbilst postsinaptiskajai daļai, un sinaptiskā plaisa, kas tos atdala (att. 14-13).
Lielos muskuļos, kas attīsta ievērojamu spēku, viens aksons, zarojoties, inervē lielu skaitu (simtiem un tūkstošiem) muskuļu šķiedru. Gluži pretēji, mazos muskuļos, kas veic smalkas kustības (piemēram, acs ārējie muskuļi), katru šķiedru vai nelielu to grupu inervē atsevišķs aksons. Viens motors neirons kopā ar tā inervētajām muskuļu šķiedrām veido motoru vienību.
presinaptiskā daļa. Muskuļu šķiedras tuvumā aksons zaudē savu mielīna apvalku un rada vairākus zarus, kas
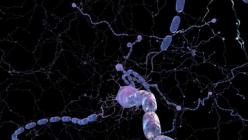
Multiplā skleroze ir vēl viens pierādījums mūsu imūnsistēmas nepilnībām, kas dažkārt “jūk prātā” un sāk uzbrukt nevis ārējam “ienaidniekam”, bet gan sava ķermeņa audiem. Šīs slimības gadījumā imūnsistēmas šūnas iznīcina nervu šķiedru mielīna apvalku, kas veidojas organisma attīstības gaitā no noteikta veida glia šūnām - nervu sistēmas "dienesta" šūnām. Mielīna apvalks aptver aksonus - garus neirona procesus, kas darbojas kā "vadi", pa kuriem virzās nervu impulss. Pats apvalks kalpo kā elektriskā izolācija, un tā iznīcināšanas rezultātā impulsa pāreja gar nervu šķiedru palēninās 5-10 reizes.
Fotoattēlā gar plāksnīšu perifēriju ir redzami makrofāgu uzkrājumi (brūnā krāsā). Makrofāgi tiek piesaistīti bojājuma vietai, un tos aktivizē citas imūnsistēmas šūnas - T-limfocīti. Aktivētie makrofāgi fagocitē ("ēd") mirstošo mielīnu, turklāt paši veicina tā bojājumus, ražojot proteāzes, pro-iekaisuma molekulas un reaktīvās skābekļa sugas. (Imūnhistoķīmija, makrofāgu marķieris - CD68).
Parasti imūnsistēmas šūnas, tāpat kā citas asins šūnas, nespēj tieši iekļūt nervu audos – tās nepieļauj tā sauktā hematoencefāliskā barjera. Bet ar multiplo sklerozi šī barjera kļūst pārvarama: “trakie” limfocīti piekļūst neironiem un to aksoniem, kur tie sāk uzbrukt mielīna molekulām, kas ir sarežģīta daudzslāņu proteīna-lipīdu struktūra. Tas izraisa molekulāru notikumu kaskādi, kas izraisa mielīna un dažreiz arī pašu aksonu iznīcināšanu.
Mielīna iznīcināšanu pavada skartās vietas iekaisuma un sklerozes attīstība, t.i. saistaudu rētas veidošanās plāksnes veidā, kas aizstāj mielīna apvalku. Attiecīgi šajā zonā tiek traucēta aksona vadošā funkcija. Plāksnes atrodas difūzi, izkaisīti pa nervu sistēmu. Tieši ar šādu bojājumu izkārtojumu ir saistīts pats slimības nosaukums - “multiplā” skleroze, kurai nav nekāda sakara ar parasto izklaidību (tā, par kuru mēs dažreiz runājam ikdienā - “Man ir pilnīga skleroze, Es atkal visu aizmirsu).
Multiplās sklerozes simptomi atšķiras un ir atkarīgi no tā, kuri nervi tiek ietekmēti. To vidū ir paralīze, līdzsvara problēmas, kognitīvie traucējumi, izmaiņas maņu orgānu darbībā (ceturtdaļai pacientu slimības attīstība sākas ar redzes traucējumiem redzes neirīta dēļ).
Mūsdienu multiplās sklerozes ārstēšana atstāj daudz vēlamo.
Pagaidām efektīvas ārstēšanas nav, jo īpaši tāpēc, ka joprojām nav zināmi šīs slimības cēloņi, ir tikai dati par iespējamo vides ietekmi un ģenētisko noslieci. Ārstēšanai papildus simptomātiskai terapijai, kas var mazināt sāpes un mazināt muskuļu spazmas, tiek izmantoti glikokortikoīdu preparāti iekaisuma mazināšanai, kā arī imūnmodulatori un imūnsupresanti, kuru mērķis ir nomākt imūnsistēmas "slikto" darbību. Visi šie līdzekļi var palēnināt slimības attīstību un samazināt paasinājumu biežumu, bet pilnībā neizārstēt pacientu. Nav zāļu, kas varētu atjaunot jau bojāto mielīnu.
Tomēr drīzumā var parādīties šādas zāles, kuru mērķis ir tieši mielīna atjaunošana, nevis tikai patoloģiskā procesa palēnināšana. Šveices uzņēmuma Biogen, lielākā multiplās sklerozes ārstēšanai paredzēto zāļu ražotāja, izstrādei ar darba nosaukumu Anti-LINGO-1 pašlaik tiek veikti 2. fāzes klīniskie pētījumi. Zāles ir monoklonāla antiviela, kas var specifiski saistīties ar LINGO-1 proteīnu, kas novērš mielinizācijas procesu un jaunu aksonu veidošanos. Attiecīgi, ja šis proteīns tiek "izslēgts", mielīns sāk atgūties.
Eksperimentos ar dzīvniekiem jauno zāļu lietošana izraisīja 90% remielinizāciju. Pacientiem ar multiplo sklerozi, kuri lieto Anti-LINGO-1, šobrīd ir uzlabojusies redzes nerva vadītspēja. Taču pilni klīnisko pētījumu rezultāti ar pacientiem tiks saņemti tikai līdz 2016. gadam.