Oamenii și vertebratele au un singur plan structural și sunt reprezentați de partea centrală - creierul și măduva spinării, precum și secțiunea periferică - nervii care se extind din organele centrale, care sunt procese ale celulelor nervoase - neuroni.
Caracteristicile celulelor neurogliale
După cum am spus deja, teaca de mielină a dendritelor și axonilor este formată din structuri speciale caracterizate printr-un grad scăzut de permeabilitate pentru ionii de sodiu și calciu și, prin urmare, având doar potențiale de repaus (nu pot conduce impulsurile nervoase și nu pot îndeplini funcții de izolare electrică).
Aceste structuri se numesc. Acestea includ:
- oligodendrocite;
- astrocite fibroase;
- celule ependimului;
- astrocite plasmatice.
Toate sunt formate din stratul exterior al embrionului - ectodermul și au un nume comun - macroglia. Gliile nervilor simpatic, parasimpatic și somatic sunt reprezentate de celule Schwann (neurolemocite).
Structura și funcțiile oligodendrocitelor
Ele fac parte din sistemul nervos central și sunt celule macrogliale. Deoarece mielina este o structură proteină-lipidă, ajută la creșterea vitezei de excitare. Celulele însele formează un strat izolator electric de terminații nervoase în creier și măduva spinării, formându-se deja în perioada de dezvoltare intrauterină. Procesele lor învelesc neuronii, precum și dendritele și axonii, în pliurile plasmalemei lor exterioare. Se dovedește că mielina este principalul material izolator electric care delimitează procesele nervoase ale nervilor mixți.

și trăsăturile lor
Învelișul de mielină a nervilor sistemului periferic este format din neurolemocite (celule Schwann). Caracteristica lor distinctivă este că sunt capabili să formeze o înveliș protector al unui singur axon și nu pot forma procese, așa cum este inerent oligodendrocitelor.
Între celulele Schwann la o distanță de 1-2 mm există zone lipsite de mielină, așa-numitele noduri ale lui Ranvier. Prin intermediul acestora, impulsurile electrice sunt efectuate spasmodic în interiorul axonului.
Lemocitele sunt capabile să repare fibrele nervoase și, de asemenea, să funcționeze.Ca urmare a aberațiilor genetice, celulele membranei lemocitelor încep diviziunea și creșterea mitotică necontrolată, în urma cărora se dezvoltă tumori - schwannoame (neurinoame) în diferite părți ale sistem nervos.
Rolul microgliei în distrugerea structurii mielinei
Microglia sunt macrofage capabile de fagocitoză și capabile să recunoască diferite particule patogene - antigene. Datorită receptorilor membranari, aceste celule gliale produc enzime - proteaze, precum și citokine, de exemplu, interleukina 1. Este un mediator al procesului inflamator și al imunității.
Teaca de mielină, a cărei funcție este de a izola cilindrul axial și de a îmbunătăți conducerea impulsului nervos, poate fi deteriorată de interleukină. Ca rezultat, nervul este „gol”, iar rata de excitare este redusă brusc.

Mai mult, citokinele, prin activarea receptorilor, provoacă transportul excesiv al ionilor de calciu în corpul neuronului. Proteazele și fosfolipazele încep să descompună organelele și procesele celulelor nervoase, ceea ce duce la apoptoză - moartea acestei structuri.
Se prăbușește, dezintegrându-se în particule, care sunt devorate de macrofage. Acest fenomen se numește excitotoxicitate. Provoacă degenerarea neuronilor și a terminațiilor acestora, ducând la boli precum boala Alzheimer și boala Parkinson.
Fibre nervoase pulpare
Dacă procesele neuronilor - dendrite și axoni, sunt acoperite cu o teacă de mielină, atunci se numesc pulpos și inervează mușchii scheletici, intrând în secțiunea somatică a sistemului nervos periferic. Fibrele nemielinice formează sistemul nervos autonom și inervează organele interne.

Procesele pulpoase au un diametru mai mare decât cele necarnoase și se formează astfel: axonii îndoaie membrana plasmatică a celulelor gliale și formează mesaxoni liniari. Apoi se alungesc, iar celulele Schwann se înfășoară în mod repetat în jurul axonului, formând straturi concentrice. Citoplasma și nucleul lemocitelor se deplasează în regiunea stratului exterior, care se numește neurilema sau membrana Schwann.
Stratul interior al lemocitelor este format dintr-un mezoxon stratificat și se numește teacă de mielină. Grosimea sa în diferite părți ale nervului nu este aceeași.
Cum se repară teaca de mielină
Având în vedere rolul microgliei în procesul de demielinizare a nervilor, am constatat că sub acțiunea macrofagelor și a neurotransmițătorilor (de exemplu, interleukinele) mielina este distrusă, ceea ce, la rândul său, duce la o deteriorare a nutriției neuronilor și la o întrerupere a transmiterii. a impulsurilor nervoase de-a lungul axonilor.
Această patologie provoacă apariția unor fenomene neurodegenerative: deteriorarea proceselor cognitive, în primul rând a memoriei și a gândirii, apariția tulburărilor de coordonare a mișcărilor corpului și a abilităților motorii fine.

Ca urmare, este posibilă o invaliditate completă a pacientului, care apare ca urmare a bolilor autoimune. Prin urmare, întrebarea cum să restabiliți mielina este în prezent deosebit de acută. Aceste metode includ în primul rând o dietă echilibrată proteico-lipidic, un stil de viață adecvat și absența obiceiurilor proaste. În cazurile severe de boli, tratamentul medicamentos este utilizat pentru a restabili numărul de celule gliale mature - oligodendrocite.
Sistemul nervos al oamenilor și al vertebratelor are un singur plan structural și este reprezentat de partea centrală - creierul și măduva spinării, precum și secțiunea periferică - pleacă de la organele centrale prin nervi, care sunt procese ale celulelor nervoase - neuroni.
Combinația lor formează țesutul nervos, ale cărui principale funcții sunt excitabilitatea și conductivitatea. Aceste proprietăți sunt explicate în primul rând prin caracteristicile structurale ale învelișurilor neuronilor și procesele lor, constând dintr-o substanță numită mielină. În acest articol, vom lua în considerare structura și funcțiile acestui compus, precum și vom afla modalități posibile de a-l restabili.
De ce neurocitele și procesele lor sunt acoperite cu mielină
Nu este o coincidență faptul că dendritele și axonii au un strat protector format din complexe proteină-lipidă. Faptul este că încălcarea este un proces biofizic, care se bazează pe impulsuri electrice slabe. Dacă curentul electric trece prin fir, atunci acesta din urmă trebuie acoperit cu material izolator pentru a reduce dispersia impulsurilor electrice și pentru a preveni scăderea puterii curentului. Teaca de mielină îndeplinește aceleași funcții în fibra nervoasă. În plus, este un suport și oferă și putere fibrei.
Compoziția chimică a mielinei
Ca majoritatea membranelor celulare, are o natură lipoproteică. Mai mult, conținutul de grăsimi aici este foarte mare - până la 75%, iar proteinele - până la 25%. Mielina conține, de asemenea, o cantitate mică de glicolipide și glicoproteine. Compoziția sa chimică diferă în nervii spinali și cranieni.
În primul, există un conținut ridicat de fosfolipide - până la 45%, iar restul cade pe colesterol și cerebrozide. Demielinizarea (adică înlocuirea mielinei cu alte substanțe în procesele nervoase) duce la astfel de boli autoimune severe, cum ar fi, de exemplu, scleroza multiplă.
Din punct de vedere chimic, acest proces va arăta astfel: teaca de mielină a fibrelor nervoase își schimbă structura, ceea ce se manifestă în primul rând printr-o scădere a procentului de lipide față de proteine. În plus, cantitatea de colesterol scade și conținutul de apă crește. Și toate acestea duc la o înlocuire treptată a mielinei, care conține oligodendrocite sau celule Schwann, macrofage, astrocite și lichid intercelular. Rezultatul unor astfel de modificări biochimice va fi o scădere bruscă a capacității axonilor de a conduce excitația până la blocarea completă a trecerii impulsurilor nervoase.
Caracteristicile celulelor neurogliale
După cum am spus deja, teaca de mielină a dendritelor și a axonilor este formată din structuri speciale care se caracterizează printr-un grad scăzut de permeabilitate pentru ionii de sodiu și calciu și, prin urmare, au doar potențiale de repaus (nu pot conduce impulsurile nervoase și nu pot îndeplini funcții de izolare electrică). ). Aceste structuri se numesc celule gliale. Acestea includ:
- oligodendrocite;
- astrocite fibroase;
- celule ependimale;
- astrocite plasmatice.
Toate sunt formate din stratul exterior al embrionului - ectodermul și au un nume comun - macroglia. Glia nervilor somatic simpatic și parasimpatic sunt reprezentate de celule Schwann (neurolemocite).
Structura și funcțiile oligodendrocitelor
Ele fac parte din sistemul nervos central și sunt celule macrogliale. Deoarece mielina este o structură proteină-lipidă, ajută la creșterea vitezei de excitare. Celulele însele formează un strat izolator electric de terminații nervoase în creier și măduva spinării, formându-se deja în perioada de dezvoltare intrauterină. Procesele lor învelesc neuronii, precum și dendritele și axonii, în pliurile plasmalemei lor exterioare. Se dovedește că mielina este principalul material izolator electric care delimitează procesele nervoase ale nervilor mixți.
Celulele Schwann și caracteristicile lor
Învelișul de mielină a nervilor sistemului periferic este format din neurolemocite (celule Schwann). Caracteristica lor distinctivă este că sunt capabili să formeze o înveliș protector al unui singur axon și nu pot forma procese, așa cum este inerent oligodendrocitelor. Între celulele Schwann la o distanță de 1-2 mm există zone lipsite de mielină, așa-numitele noduri ale lui Ranvier. În spatele acestuia, impulsurile electrice sunt efectuate spasmodic în interiorul axonului. Lemocitele sunt capabile să repare fibrele nervoase și, de asemenea, îndeplinesc o funcție trofică. Ca urmare a aberațiilor genetice, celulele învelișului lemocitelor încep diviziunea și creșterea mitotică necontrolată, în urma cărora se dezvoltă tumori, schwannoame (neurinoame), în diferite părți ale sistemului nervos.
Rolul microgliei în distrugerea structurii mielinei
Microglia sunt macrofage capabile de fagocitoză și sunt capabile să recunoască diferite particule patogene - antigene. Datorită receptorilor membranari, aceste celule gliale produc enzime - proteaze, precum și citokine, de exemplu, interleukina 1. Este un mediator al procesului inflamator și al imunității. Teaca de mielină, a cărei funcție este de a izola cilindrul axial și de a îmbunătăți conducerea impulsului nervos, poate fi deteriorată de interleukină. Ca rezultat, nervul este „expus” și viteza de conducere a excitației este redusă brusc.
Mai mult, citokinele, prin activarea receptorilor, provoacă transportul excesiv al ionilor de calciu în corpul neuronului. Proteazele și fosfolipazele încep să descompună organelele și procesele celulelor nervoase, ceea ce duce la apoptoză - moartea acestei structuri. Se prăbușește, dezintegrându-se în particule, care sunt devorate de macrofage. Acest fenomen se numește excitotoxicitate. Provoacă degenerarea neuronilor și a terminațiilor acestora, ducând la boli precum boala Alzheimer și boala Parkinson.
Fibre nervoase pulpare
Dacă procesele neuronilor - dendrite și axoni, sunt acoperite cu o teacă de mielină, atunci se numesc pulpos și inervează mușchii scheletici, intrând în secțiunea somatică a sistemului nervos periferic. Fibrele nemielinice formează sistemul nervos autonom și inervează organele interne.
Procesele pulpe au un diametru mai mare decât procesele nepulmonice și se formează astfel: axonii îndoaie membrana plasmatică a celulelor gliale și formează mesaxoni liniari. Apoi se măresc și celulele Schwann se înfășoară în mod repetat în jurul axonului, formând straturi concentrice. Citoplasma și nucleul lemocitelor se deplasează în regiunea stratului exterior, care se numește neurilema sau membrana Schwann. Stratul interior al lemocitelor este format dintr-un mezoxon stratificat și se numește teacă de mielină. Grosimea sa în diferite părți ale nervului nu este aceeași.
Cum se repară teaca de mielină
Având în vedere rolul microgliei în procesul de demielinizare a nervilor, am constatat că sub acțiunea macrofagelor și a neurotransmițătorilor (de exemplu, interleukinele) mielina este distrusă, ceea ce, la rândul său, duce la o deteriorare a nutriției neuronilor și la o încălcare a transmiterii. a impulsurilor nervoase de-a lungul axonilor. Această patologie provoacă apariția unor fenomene neurodegenerative: deteriorarea proceselor cognitive, în primul rând a memoriei și a gândirii, apariția tulburărilor de coordonare a mișcărilor corpului și a abilităților motorii fine.
Ca urmare, este posibilă o invaliditate completă a pacientului, care apare ca urmare a bolilor autoimune. Prin urmare, întrebarea cum să restabiliți mielina este în prezent deosebit de acută. Aceste metode includ, în primul rând, o dietă echilibrată proteico-lipidic, un stil de viață adecvat și absența obiceiurilor proaste. În cazurile severe de boli, tratamentul medicamentos este utilizat pentru a restabili numărul de celule gliale mature - oligodendrocite.
Data publicării: 26/05/17Sistemul nervos central (SNC) este un singur mecanism care este responsabil pentru percepția lumii înconjurătoare și a reflexelor, precum și pentru controlul sistemului de organe și țesuturi interne. Ultimul punct este realizat de partea periferică a sistemului nervos central cu ajutorul unor celule speciale numite neuroni. Țesutul nervos este format din ele, care servește la transmiterea impulsurilor.
Procesele care vin din corpul neuronului sunt înconjurate de un strat protector care hrănește fibrele nervoase și accelerează transmiterea impulsurilor, iar o astfel de protecție se numește înveliș de mielină. Orice semnal transmis prin fibrele nervoase seamănă cu o descărcare de curent, iar stratul lor exterior nu permite scăderea puterii sale.
Dacă teaca de mielină este deteriorată, atunci percepția completă în această parte a corpului se pierde, dar celula poate supraviețui, iar daunele se vindecă în timp. Cu leziuni suficient de grave, vor fi necesare medicamente concepute pentru a restabili fibrele nervoase precum Milgamma, Copaxone și altele. În caz contrar, nervul va muri în cele din urmă și percepția va scădea. Bolile care se caracterizează prin această problemă includ radiculopatia, polineuropatia etc., dar medicii consideră scleroza multiplă (SM) drept cel mai periculos proces patologic. În ciuda numelui ciudat, boala nu are nimic de-a face cu definiția directă a acestor cuvinte și înseamnă „cicatrici multiple” în traducere. Acestea apar pe teaca de mielină din măduva spinării și creier din cauza insuficienței imune, astfel încât SM este o boală autoimună. În locul fibrelor nervoase, la locul focarului apare o cicatrice, constând din țesut conjunctiv, prin care impulsul nu mai poate trece corect.
Este posibil să restabiliți cumva țesutul nervos deteriorat sau va rămâne pentru totdeauna într-o stare infirmă? Medicii încă nu pot răspunde cu exactitate și încă nu au venit cu un medicament cu drepturi depline pentru a restabili sensibilitatea la terminațiile nervoase. În schimb, există diverse medicamente care pot reduce procesul de demielinizare, pot îmbunătăți nutriția zonelor deteriorate și pot activa regenerarea tecii de mielină.
Milgamma este un neuroprotector pentru restabilirea metabolismului în interiorul celulelor, ceea ce vă permite să încetiniți procesul de distrugere a mielinei și să începeți regenerarea acesteia. Medicamentul se bazează pe vitamine din grupa B și anume:
- Tiamina (B1). Este esențială pentru absorbția zahărului în organism și a energiei. Cu deficiența acută de tiamină la o persoană, somnul este perturbat și memoria se deteriorează. Devine nervos și uneori deprimat, ca în depresie. În unele cazuri, apar simptome de parestezie (pielea de găină, scăderea sensibilității și furnicături în vârful degetelor);
- Piridoxina (B6). Această vitamină joacă un rol important în producerea de aminoacizi, precum și a unor hormoni (dopamină, serotonina etc.). În ciuda cazurilor rare de lipsă de piridoxină în organism, din cauza deficienței sale, este posibilă o scădere a abilităților mentale și o slăbire a apărării imune;
- Cianocobalamina (B12). Servește la îmbunătățirea conductivității fibrelor nervoase, rezultând o sensibilitate îmbunătățită, precum și la îmbunătățirea sintezei sângelui. Cu o lipsă de cianocobalamină, o persoană dezvoltă halucinații, demență (demență), există întreruperi ale ritmului cardiac și parestezii.
Datorită acestei compoziții, Milgama este capabilă să oprească oxidarea celulelor de către radicalii liberi (substanțe reactive), care vor afecta restabilirea sensibilității țesuturilor și a terminațiilor nervoase. După un curs de administrare a comprimatelor, există o scădere a simptomelor și o îmbunătățire a stării generale, iar medicamentul trebuie administrat în 2 etape. În prima, va trebui să faceți cel puțin 10 injecții, apoi să treceți la tablete (Milgamma compositum) și să le luați de 3 ori pe zi timp de 1,5 luni.

Sulfatul de stafaglabrină a fost folosit de mult timp pentru a restabili sensibilitatea țesuturilor și a fibrelor nervoase în sine. Planta din ale cărei rădăcini este extras acest medicament crește numai în climatele subtropicale și tropicale, de exemplu, în Japonia, India și Birmania, și se numește Stephania netedă. Există cazuri de obținere a sulfatului de Stafaglabrin în laborator. Poate că acest lucru se datorează faptului că stephania netedă poate fi cultivată ca cultură în suspensie, adică într-o poziție suspendată în baloane de sticlă cu lichid. În sine, medicamentul este o sare sulfat, care are un punct de topire ridicat (mai mult de 240 ° C). Se referă la alcaloidul (compusul care conține azot) stefarină, care este considerată baza pentru proaporfină.
Sulfatul de stefaglabrină servește la reducerea activității enzimelor din clasa hidrolazelor (colinesterază) și la îmbunătățirea tonusului mușchilor netezi care sunt prezenți în pereții vaselor de sânge, ai organelor (cav în interior) și a ganglionilor limfatici. De asemenea, se știe că medicamentul este ușor toxic și poate reduce tensiunea arterială. Pe vremuri, medicamentul era folosit ca agent anticolinesterazic, dar apoi oamenii de știință au ajuns la concluzia că sulfatul de Stefaglabrin este un inhibitor al activității de creștere a țesutului conjunctiv. Din aceasta rezultă că își întârzie dezvoltarea și nu se formează cicatrici pe fibrele nervoase. De aceea, medicamentul a început să fie utilizat în mod activ pentru deteriorarea PNS.
În timpul cercetării, experții au putut observa creșterea celulelor Schwann, care produc mielină în sistemul nervos periferic. Acest fenomen înseamnă că, sub influența medicamentului, pacientul îmbunătățește semnificativ conducerea impulsului de-a lungul axonului, deoarece teaca de mielină a început din nou să se formeze în jurul său. De când s-au obținut rezultatele, medicamentul a devenit o speranță pentru multe persoane diagnosticate cu patologii demielinizante incurabile.

Problema patologiei autoimune nu va fi posibilă doar prin refacerea fibrelor nervoase. Într-adevăr, indiferent de câte focare de daune trebuie eliminate, problema va reveni, deoarece sistemul imunitar reacționează la mielină ca un corp străin și îl distruge. Până în prezent, este imposibil să se elimine un astfel de proces patologic, dar nu se mai poate întreba dacă fibrele nervoase sunt restaurate sau nu. Oamenii sunt lăsați să își mențină starea prin suprimarea sistemului imunitar și folosind medicamente precum sulfatul de Stefaglabrin pentru a-și menține sănătatea.
Medicamentul poate fi utilizat numai parenteral, adică prin intestine, de exemplu, prin injecție. Doza în acest caz nu trebuie să depășească 7-8 ml de soluție de 0,25% pe zi pentru 2 injecții. Judecând după timp, teaca de mielină și terminațiile nervoase sunt de obicei restaurate într-o oarecare măsură după 20 de zile, apoi aveți nevoie de o pauză și puteți înțelege cât va dura, după ce ați aflat despre asta de la medic. Cel mai bun rezultat, potrivit medicilor, poate fi obținut în detrimentul dozelor mici, deoarece efectele secundare se dezvoltă mult mai puțin frecvent, iar eficacitatea tratamentului crește.
În condiții de laborator, la timp pentru experimente pe șobolani, s-a constatat că, cu o concentrație a medicamentului sulfat de Stefaglabrin de 0,1-1 mg / kg, tratamentul este mai rapid decât fără acesta. Cursul terapiei sa încheiat mai devreme, în comparație cu animalele care nu au luat acest medicament. După 2-3 luni, fibrele nervoase la rozătoare au fost aproape complet restaurate, iar impulsul a fost transmis de-a lungul nervului fără întârziere. La subiecții experimentali care au fost tratați fără acest medicament, recuperarea a durat aproximativ șase luni și nu toate terminațiile nervoase au revenit la normal.
Copaxone

Nu există un remediu pentru scleroza multiplă, dar există medicamente care pot reduce efectul sistemului imunitar asupra tecii de mielină, iar Copaxone este unul dintre ele. Esența bolilor autoimune este că sistemul imunitar distruge mielina situată pe fibrele nervoase. Din această cauză, conductivitatea impulsurilor se înrăutățește, iar Copaxone este capabil să schimbe obiectivul sistemului de apărare al organismului în sine. Fibrele nervoase rămân intacte, dar dacă celulele corpului au preluat deja eroziunea tecii de mielină, atunci medicamentul le va putea împinge înapoi. Acest fenomen apare din cauza faptului că medicamentul este foarte asemănător ca structură cu mielina, astfel încât sistemul imunitar își atrage atenția asupra acestuia.
Medicamentul este capabil nu numai să preia atacul sistemului de apărare al organismului, ci și să producă celule speciale ale sistemului imunitar pentru a reduce intensitatea bolii, care sunt numite limfocite Th2. Mecanismul influenței și formării lor nu a fost încă studiat corespunzător, dar există diverse teorii. Există o opinie printre experți că celulele dendritice ale epidermei sunt implicate în sinteza limfocitelor Th2.
Limfocitele supresoare (mutate) dezvoltate, care intră în sânge, pătrund rapid în partea sistemului nervos unde se află focarul inflamației. Aici, limfocitele Th2, datorită influenței mielinei, produc citokine, adică molecule antiinflamatorii. Încep să amelioreze treptat inflamația din această parte a creierului, îmbunătățind astfel sensibilitatea terminațiilor nervoase.
Beneficiul medicamentului nu este numai pentru tratamentul bolii în sine, ci și pentru celulele nervoase în sine, deoarece Copaxone este un neuroprotector. Efectul protector se manifestă prin stimularea creșterii celulelor creierului și îmbunătățirea metabolismului lipidic. Învelișul de mielină constă în principal din lipide, iar în multe procese patologice asociate cu deteriorarea fibrelor nervoase are loc oxidarea acestora, astfel încât mielina este deteriorată. Medicamentul Copaxone este capabil să elimine această problemă, deoarece crește antioxidantul natural al organismului (acid uric). Din cauza creșterii nivelului de acid uric nu se știe, dar acest fapt a fost dovedit în cursul a numeroase experimente.
Medicamentul servește la protejarea celulelor nervoase și la reducerea severității și frecvenței exacerbărilor. Poate fi combinat cu medicamentele sulfat de Stefaglabrin și Milgamma.
Învelișul de mielină va începe să se recupereze datorită creșterii crescute a celulelor Schwann, iar Milgamma va îmbunătăți metabolismul intracelular și va spori efectul ambelor medicamente. Este strict interzis să le folosești singure sau să schimbi singur doza.
Este posibil să restabiliți celulele nervoase și cât timp va dura doar un specialist poate răspunde, concentrându-se pe rezultatele examinării. Este interzis să luați singur medicamente pentru a îmbunătăți sensibilitatea țesuturilor, deoarece majoritatea au o bază hormonală, ceea ce înseamnă că sunt greu de tolerat de către organism.
FIBRE NERVIVE
Fibrele nervoase sunt procese ale neuronilor acoperiți cu teci gliale. Există două tipuri de fibre nervoase - nemielinizate și mielinice. Ambele tipuri constau într-un proces central al unui neuron (un cilindru axial) înconjurat de o teacă de celule oligodendroglie (în SNP sunt numite lemocite sau celule Schwann).
fibre nervoase nemielinice la un adult, ele sunt localizate în principal în sistemul nervos autonom și se caracterizează printr-o viteză relativ scăzută a conducerii impulsului nervos (0.5-2 Domnișoară). Ele se formează prin scufundarea cilindrului axial (axonul) în citoplasma lemocitelor, care sunt situate sub formă de fire. În acest caz, plasmolema lemocitelor se îndoaie, înconjoară axonul și formează o duplicare - mesaxonul (Fig. 14-7). Adesea, în citoplasma unui lemocit poate exista până la 10-20 cilindri de osie. O astfel de fibră seamănă cu un cablu electric și, prin urmare, este numită fibră de tip cablu. Suprafața fibrei este acoperită cu o membrană bazală. În SNC, în special în cursul dezvoltării sale, sunt descrise fibre nemielinice, constând dintr-un axon „gol”, lipsit de o teacă de lemocite.
Orez. 14-7. Formarea fibrelor nervoase mielinice (1-3) și nemielinice (4) în sistemul nervos periferic. Fibra nervoasă se formează prin scufundarea axonului (A) al celulei nervoase în citoplasma lemocitelor (LC). Atunci când se formează o fibră de mielină, o duplicare a plasmolemei LC - mesaxon (MA) - este înfășurată în jurul lui A, formând spire ale tecii de mielină (MO). În fibra fără mielină prezentată în figură, mai mulți A sunt scufundați în citoplasma LC (fibră de tip cablu). Eu sunt nucleul LC.

fibre nervoase mielinice găsite în SNC și SNP și se caracterizează printr-o viteză mare de conducere a impulsului nervos (5-120 Domnișoară). Fibrele mielinice sunt de obicei mai groase decât cele nemielinizate și conțin cilindri axiali cu diametru mai mare. În fibra de mielină, cilindrul axial este înconjurat direct de o teacă specială de mielină, în jurul căreia există un strat subțire care include citoplasma și nucleul lemocitelor - neurolema (Fig. 14-8 și 14-9). În exterior, fibra este acoperită și cu o membrană bazală. Învelișul de mielină conține concentrații mari de lipide și este colorat intens cu acid osmic, având aspectul unui strat omogen la microscop optic, dar la microscop electronic se constată că aceasta ia naștere ca urmare a fuziunii a numeroase (până la 300) bobine de membrană (plăci).
Orez. 14-8. Structura fibrei nervoase mielinice. Fibra de mielină este formată dintr-un cilindru axial sau axon (A), înconjurat direct de o teacă de mielină (MO) și o neurolemă (NL), inclusiv citoplasma (CL) și nucleul lemocitelor (NL). În exterior, fibra este acoperită cu o membrană bazală (BM). Zonele de MO, în care se păstrează golurile dintre spirele de mielină, umplute cu CL și, prin urmare, necolorate cu osmiu, au forma unor crestături de mielină (MN).
Formarea tecii de mielină apare în timpul interacțiunii dintre cilindrul axial și celulele oligodendrogliei cu unele diferențe în SNP și SNC.
Formarea tecii de mielină în SNP : imersarea cilindrului axial în lemocit este însoțită de formarea unui mesaxon lung, care începe să se rotească în jurul axonului, formând primele spire aranjate liber ale tecii de mielină (vezi Fig. 14-7). Pe măsură ce numărul de spire (plăci) crește în procesul de maturare a mielinei, acestea sunt aranjate din ce în ce mai dens și se contopesc parțial; golurile dintre ele, umplute cu citoplasma lemocitelor, sunt păstrate numai în zone separate care nu sunt colorate cu crestături de osmiu - mielină (Schmidt-Lanterman). În timpul formării tecii de mielină, citoplasma și nucleul lemocitelor sunt împinse la periferia fibrei, formând neurolema. Învelișul de mielină are un curs discontinuu pe lungimea fibrei.

Orez. 14-9. Organizarea ultrastructurală a fibrei nervoase mielinice. În jurul axonului (A) se află bobine ale tecii de mielină (MMO), acoperite extern cu o neurolemă, și care include citoplasma (CL) și nucleul lemocitelor (NL). Fibra este înconjurată la exterior de o membrană bazală (BM). CL, pe lângă neurolemă, formează o foaie interioară (IL) direct adiacentă lui A (situată între acesta și SMO), este, de asemenea, conținută în zona corespunzătoare graniței lemocitelor învecinate - interceptarea ganglionilor (NC), acolo unde teaca de mielină este absentă, iar în zonele de stivuire WMO libere - crestături de mielină (MN).
Interceptări nodale (Ranvier)- zone din regiunea graniței lemocitelor învecinate, în care teaca de mielină este absentă, iar axonul este acoperit doar de procese de interdigitare ale lemocitelor învecinate (vezi Fig. 14-9). Interceptările nodale se repetă de-a lungul cursului fibrei de mielină cu un interval egal, în medie, cu 1-2 mm. În regiunea nodului nodal, axonul se extinde adesea, iar plasmolema sa conține numeroase canale de sodiu (care sunt absente în afara nodurilor de sub teaca de mielină).
Propagarea depolarizării în fibra de mielină efectuate în sărituri de la interceptare la interceptare (saltatorie). Depolarizarea în regiunea unei joncțiuni nodale este însoțită de propagarea sa pasivă rapidă de-a lungul axonului până la următoarea joncțiune (deoarece scurgerea curentului în regiunea internodală este minimă datorită proprietăților izolatoare ridicate ale mielinei). În zona următoarei interceptări, impulsul determină pornirea canalelor ionice existente și apare o nouă zonă de depolarizare locală etc.
Formarea tecii de mielină în SNC: cilindrul axial nu se scufundă în citoplasma oligodendrocitelor, ci este acoperit de procesul său plat, care ulterior se rotește în jurul lui, pierzând citoplasma, iar bobinele sale se transformă în plăci ale tecii de mielină.

coate (Fig. 14-10). Spre deosebire de celulele Schwann, un oligodendrocit al SNC cu procesele sale poate participa la mielinizarea multor (până la 40-50) fibre nervoase. Siturile axonilor din zona nodurilor lui Ranvier din SNC nu sunt acoperite de citoplasma oligodendrocitelor.
Orez. 14-10. Formarea fibrelor de mielină de către oligodendrocite din SNC. 1 - axonul (A) neuronului este acoperit de un proces plat (PO) al oligodendrocitelor (ODC), ale cărui bobine se transformă în plăci ale tecii de mielină (MO). 2 - un ODC cu procesele sale poate participa la mielinizarea multor A. Zonele A din zona interceptărilor nodale (NC) nu sunt acoperite de citoplasma ODC.
Încălcarea formării și deteriorarea mielinei formate stau la baza o serie de boli grave ale sistemului nervos. Mielina din SNC poate fi o țintă pentru daune autoimune limfocitele T iar macrofagele cu distrugerea acesteia (demielinizare). Acest proces se desfășoară în mod activ în scleroza multiplă, o boală gravă de natură neclară (probabil virală), asociată cu o tulburare a diferitelor funcții, dezvoltarea paraliziei și pierderea sensibilității. Natura tulburărilor neurologice este determinată de topografia și dimensiunea zonelor afectate. Cu unele tulburări metabolice, există tulburări în formarea mielinei - leucodistrofie, manifestată în copilărie prin leziuni severe ale sistemului nervos.
Clasificarea fibrelor nervoase
Clasificarea fibrelor nervoase se bazează pe diferențele de structură și funcție (viteza impulsurilor nervoase). Există trei tipuri principale de fibre nervoase:
1. Fibre de tip A - gros, mielinizat, cu interceptări nodale la distanță. Conduce impulsurile la viteză mare
(15-120 m/s); subdivizat în 4 subtipuri (α, β, γ, δ) cu diametrul și viteza de conducere a impulsurilor descrescătoare.
2. Fibre de tip B - grosime medie, mielina, diametru mai mic,
decât fibrele de tip A, cu o teacă de mielină mai subțire și o viteză mai mică de conducere a impulsului nervos (5-15 m/s).
3. Fibre de tip C - subțiri, nemielinice, conduce impulsurile la o viteză relativ mică(0,5-2 m/s).
Regenerarea fibrelor nervoase în SNP include o secvență complexă de procese care se desfășoară în mod natural în timpul căreia procesul neuronal interacționează activ cu celulele gliale. Regenerarea efectivă a fibrelor urmează o serie de modificări reactive cauzate de deteriorarea acestora.
Modificări reactive ale fibrei nervoase după transecția acesteia. În prima săptămână după tăierea fibrei nervoase se dezvoltă degenerarea ascendentă a părții proximale (cea mai apropiată de corpul neuronului) a axonului, la capătul căreia se formează o extensie (balon de retracție). Teaca de mielină din zona afectată se dezintegrează, corpul neuronului se umflă, nucleul se deplasează la periferie, substanța cromatofilă se dizolvă (Fig. 14-11).
În partea distală a fibrei, după secțiunea ei, se observă degenerarea descendentă cu distrugerea completă a axonului, descompunerea mielinei și fagocitoza ulterioară a detritusului de către macrofage și glia.
Transformări structurale în timpul regenerării fibrei nervoase. După 4-6 săptămâni. structura și funcția neuronului sunt restabilite, din balonul de retracție încep să crească ramuri subțiri (conuri de creștere) în direcția părții distale a fibrei. Celulele Schwann din partea proximală a fibrei proliferează, formând panglici (Büngner) paralele cu cursul fibrei. În partea distală a fibrei, celulele Schwann persistă și se divid mitotic, formând panglici care se conectează cu formațiuni similare în partea proximală.
Axonul în regenerare crește în direcția distală cu o rată de 3-4 mm/zi. de-a lungul benzilor Büngner, care joacă un rol de susținere și îndrumare; Celulele Schwann formează o nouă înveliș de mielină. Colateralele și terminalele axonale sunt restaurate în câteva luni.

Orez. 14-11. Regenerarea fibrei nervoase mielinice (după R.Krstic, 1985, cu modificări). 1 - după transecția fibrei nervoase, partea proximală a axonului (A) suferă degenerescență ascendentă, teaca de mielină (MO) din zona afectată se dezintegrează, pericarionul (PC) neuronului se umflă, nucleul se deplasează la periferie, substanța cromatofilă (CS) se dezintegrează (2). Partea distală asociată cu organul inervat (în exemplul dat, mușchiul scheletic) suferă degenerare descendentă cu distrugerea completă a A, dezintegrarea MO și fagocitoza detritusului de către macrofage (MF) și glia. Lemocitele (LC) persistă și se divid mitotic, formând fire - panglicile lui Büngner (LB), conectându-se cu formațiuni similare în partea proximală a fibrei (săgeți subțiri). După 4-6 săptămâni, structura și funcția neuronului sunt restabilite, ramurile subțiri cresc distal de partea proximală A (săgeata aldine), crescând de-a lungul LB (3). Ca urmare a regenerării fibrei nervoase, conexiunea cu organul țintă (mușchiul) este restabilită și atrofia acesteia cauzată de afectarea inervației regresează (4). În cazul unei obstacole (P) pe calea regenerării A (de exemplu, o cicatrice a țesutului conjunctiv), componentele fibrei nervoase
formează un neurom traumatic (TN), care constă din ramuri în creștere A și LC (5).
conditii de regenerare sunt: nicio afectare a corpului neuronului, o distanță mică între părțile fibrei nervoase, absența țesutului conjunctiv care poate umple golul dintre părțile fibrei. Când apare o obstrucție pe calea axonului în regenerare, se formează un neurom traumatic (amputație), care constă dintr-un axon în creștere și celule Schwann lipite în țesutul conjunctiv.
Nu există regenerare a fibrelor nervoase în SNC : deși neuronii SNC au capacitatea de a-și restabili procesele, acest lucru nu se întâmplă, aparent datorită influenţei adverse a micromediului. După deteriorarea unui neuron, microglia, astrocitele și macrofagele hematogene fagocitează detritus în zona fibrei distruse, iar astrocitele în proliferare formează o cicatrice glială densă în locul său.
TERMINAȚII NERVOASE
Terminații nervoase- dispozitivele terminale ale fibrelor nervoase. În funcție de funcția lor, acestea sunt împărțite în trei grupuri:
1) contacte interneuronale (sinapse)- asigura o conexiune functionala intre neuroni;
2) terminații eferente (efectoare).- transmit semnale de la sistemul nervos către organele executive (mușchi, glande), sunt prezente pe axoni;
3) terminații receptor (sensibile).percep iritatii din mediul extern si intern, sunt prezente pe dendrite.
CONTACTE INTERNEURONALE (SYNAPSE)
Contacte interneuronale (sinapse)împărțite în electrice și chimice.
sinapsele electrice rar în SNC al mamiferelor; au structura joncțiunilor gap, în care membranele celulelor conectate sinaptic (pre- și postsinaptice) sunt separate printr-un interval de 2 nm lățime străpuns de conexoni. Acestea din urmă sunt tuburi formate din molecule de proteine și servesc drept canale de apă prin care moleculele mici și ionii pot fi transportate de la o celulă la alta.

altul (vezi capitolul 3). Atunci când un potențial de acțiune care se propagă prin membrana unei celule ajunge la joncțiunea golului, un curent electric trece pasiv prin spațiu de la o celulă la alta. Impulsul poate fi transmis în ambele direcții și practic fără întârziere.
Sinapsele chimice- cel mai frecvent tip la mamifere. Acțiunea lor se bazează pe conversia unui semnal electric într-un semnal chimic, care este apoi convertit înapoi într-un semnal electric. Sinapsa chimică este formată din trei componente: partea presinaptică, partea postsinaptică și despicatură sinaptică (Fig. 14-12). Partea presinaptică conține un (neuro)transmițător, care, sub influența unui impuls nervos, este eliberat în fanta sinaptică și, legându-se de receptorii din partea postsinaptică, provoacă modificări ale permeabilității ionice a membranei sale, ceea ce duce la depolarizare (în sinapsele excitatorii) sau hiperpolarizarea (în sinapsele inhibitorii). ). Sinapsele chimice diferă de sinapsele electrice prin conducerea unilaterală a impulsurilor, o întârziere în transmiterea lor (o întârziere sinaptică de 0,2-0,5 ms) și asigurarea atât a excitației, cât și a inhibării neuronului postsinaptic.
Orez. 14-12. Structura unei sinapse chimice. Partea presinaptică (PRSP) are forma unui buton terminal (CB) și include: vezicule sinaptice (SP), mitocondrii (MTX), neurotubuli (NT), neurofilamente (NF), membrană presinaptică (PRSM) cu compactare presinaptică (PRSU). ). Partea postsinaptică (PSCH) include membrana postsinaptică (POSM) cu compactarea postsinaptică (POSU). Despicatură sinaptică (SC) conține filamente intrasinaptice (ISF).
1. partea presinaptică este format de axon de-a lungul cursului său (sinapsa care trece) sau este o parte terminală extinsă a axonului (mugurul terminal). Contine mitocondrii, AER, neurofilamente, neurotubuli si vezicule sinaptice cu diametrul de 20-65 nm, care contin neurotransmitatorul. Forma și natura conținutului veziculelor depind de neurotransmițătorii din ele. Veziculele ușoare rotunde conțin de obicei acetilcolină, vezicule cu un centru compact dens - norepinefrină, vezicule mari dense cu o margine submembrană ușoară - peptide. Neurotransmițătorii sunt produși în corpul neuronului și sunt transportați la terminațiile axonilor prin mecanismul de transport rapid, unde sunt depuși. Parțial, veziculele sinaptice se formează în sinapsa însăși prin desprinderea din cisternele AER. Pe partea interioară a plasmolemei, cu fața spre fanta sinaptică (membrană presinaptică), există un sigiliu presinaptic format dintr-o rețea de proteine hexagonale fibrilare, ale cărei celule contribuie la o distribuție uniformă a veziculelor sinaptice pe suprafața membranei.
2. partea postsinaptică Este reprezentat de o membrană postsinaptică care conține complexe speciale de proteine integrale - receptori sinaptici care se leagă de un neurotransmițător. Membrana este îngroșată din cauza acumulării de material proteic filamentos dens sub ea (compactare postsinaptică). În funcție de faptul că partea postsinaptică a sinapsei interneuronale este dendrita, corpul neuronului sau (mai rar) axonul acestuia, sinapsele sunt împărțite în axo-dendritice, axosomatice și respectiv axo-axonale.
3. despicatură sinaptică Lățimea de 20-30 nm conține uneori filamente intrasinaptice de glicoproteină transversală de 5 nm grosime, care sunt elemente ale unui glicocalix specializat care asigură legături adezive ale părților pre- și postsinatice, precum și difuzia direcționată a mediatorului.
Mecanismul de transmitere a unui impuls nervos într-o sinapsă chimică. Sub influența unui impuls nervos, sunt activate canalele de calciu dependente de tensiune ale membranei presinaptice; Sa 2+ se grăbește spre axon, membranele veziculelor sinaptice în prezența Ca2+ se contopesc cu membrana presinaptică, iar conținutul lor (mediatorul) este eliberat în fanta sinaptică prin mecanismul exocitozei. Acționând asupra receptorilor membranei postsinaptice, mediatorul provoacă fie depolarizarea acesteia, apariția unui potențial de acțiune postsinaptic și formarea unui impuls nervos, fie hiperpigmentarea acestuia.
polarizare, provocând un răspuns inhibitor. Mediatorii excitatori, de exemplu, sunt acetilcolina și glutamatul, în timp ce inhibarea este mediată de GABA și glicină.
După terminarea interacțiunii mediatorului cu receptorii membranei postsinaptice, cea mai mare parte a endocitozei sale este captată de partea presinaptică, partea mai mică este împrăștiată în spațiu și capturată de celulele gliale din jur. Unii mediatori (de exemplu, acetilcolina) sunt descompuși de enzime în componente care sunt apoi capturate de partea presinaptică. Membranele veziculelor sinaptice înglobate în membrana presinaptică sunt în continuare încorporate în vezicule căptușite endocitare și reutilizate pentru a forma noi vezicule sinaptice.
În absența unui impuls nervos, partea presinaptică eliberează mici porțiuni individuale ale mediatorului, provocând potențiale miniaturale spontane în membrana postsinaptică.
TERMINAȚII NERVIVE EFFERENTE (EFECTOR).
Terminații nervoase eferente (efectoare). În funcție de natura organului inervat, ele se împart în motorii și secretori. Terminațiile motorii se găsesc în mușchii striați și netezi, secretori - în glande.
Terminație neuromusculară (joncțiune neuromusculară, placă motorie) - terminația motorie a axonului neuronului motor de pe fibrele mușchilor somatici striați - constă din ramificarea terminală a axonului, care formează partea presinaptică, o zonă specializată pe fibra musculară, corespunzătoare părții postsinaptice, și fanta sinaptică care le separă (Fig. 14-13).
În mușchii mari care dezvoltă o forță semnificativă, un axon, ramificat, inervează un număr mare (sute și mii) de fibre musculare. Dimpotrivă, în mușchii mici care efectuează mișcări fine (de exemplu, mușchii externi ai ochiului), fiecare fibră sau un grup mic al acestora este inervată de un axon separat. Un neuron motor, împreună cu fibrele musculare inervate de acesta, formează o unitate motorie.
partea presinaptică.În apropierea fibrei musculare, axonul își pierde teaca de mielină și dă naștere mai multor ramuri care
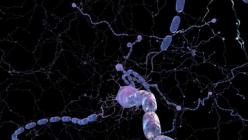
Scleroza multiplă este o altă dovadă a imperfecțiunii sistemului nostru imunitar, care uneori „înnebunește” și începe să atace nu un „inamic” extern, ci țesuturile propriului corp. În această boală, celulele sistemului imunitar distrug învelișul de mielină a fibrelor nervoase, care se formează în timpul dezvoltării corpului dintr-un anumit tip de celule gliale - celule „de serviciu” ale sistemului nervos. Învelișul de mielină acoperă axonii - procese lungi ale unui neuron care acționează ca „fire” prin care circulă un impuls nervos. Învelișul în sine servește ca izolație electrică și, ca urmare a distrugerii sale, trecerea unui impuls de-a lungul fibrei nervoase încetinește de 5-10 ori.
În fotografie, acumulări de macrofage (culoare maro) sunt vizibile de-a lungul periferiei plăcilor. Macrofagele sunt atrase de leziune și activate de alte celule ale sistemului imunitar - limfocitele T. Macrofagele activate fagocitează („mănâncă”) mielina muribundă și, în plus, ele înșiși contribuie la deteriorarea acesteia, producând proteaze, molecule proinflamatorii și specii reactive de oxigen. (Imunohistochimie, marker macrofagic - CD68).
În mod normal, celulele sistemului imunitar, ca și alte celule sanguine, nu sunt capabile să pătrundă direct în țesutul nervos - nu sunt permise de așa-numita barieră hemato-encefalică. Dar cu scleroza multiplă, această barieră devine acceptabilă: limfocitele „nebunești” au acces la neuroni și axonii lor, unde încep să atace moleculele de mielină, care sunt o structură complexă proteină-lipidă multistrat. Acest lucru declanșează o cascadă de evenimente moleculare care duc la distrugerea mielinei și uneori a axonilor înșiși.
Distrugerea mielinei este însoțită de dezvoltarea inflamației și a sclerozei zonei afectate, adică. formarea unei cicatrici de țesut conjunctiv sub forma unei plăci care înlocuiește teaca de mielină. În consecință, în această zonă, funcția conductivă a axonului este afectată. Plăcile sunt localizate difuz, împrăștiate în tot sistemul nervos. Cu această aranjare a leziunilor este asociat chiar numele bolii - scleroza „multiple”, care nu are nimic de-a face cu distracția obișnuită (cea despre care vorbim uneori în viața de zi cu zi - „Am scleroză completă, Am uitat totul din nou”).
Simptomele sclerozei multiple variază și depind de nervii afectați. Printre acestea se numără paralizia, problemele de echilibru, tulburările cognitive, modificările funcționării organelor de simț (la un sfert dintre pacienți, dezvoltarea bolii începe cu deficiența vizuală din cauza nevritei optice).
Tratamentul modern al sclerozei multiple lasa mult de dorit.
Nu există încă un tratament eficient, mai ales că încă nu se cunosc cauzele acestei boli, există doar date despre posibila influență a mediului și predispoziție genetică. Pentru tratament, pe lângă terapia simptomatică, care poate ameliora durerea și reduce spasmele musculare, preparatele cu glucocorticoizi sunt utilizate pentru a reduce inflamația, precum și imunomodulatorii și imunosupresoarele care vizează suprimarea activității „rele” a sistemului imunitar. Toate aceste remedii pot încetini dezvoltarea bolii și pot reduce frecvența exacerbărilor, dar nu vindecă complet pacientul. Nu există medicamente care să poată repara mielina deja deteriorată.
Cu toate acestea, un astfel de medicament, care vizează în mod special restabilirea mielinei și nu doar încetinirea procesului patologic, poate apărea în curând. Dezvoltarea sub titlul de lucru Anti-LINGO-1 de la compania elvețiană Biogen, cel mai mare producător de medicamente pentru tratamentul sclerozei multiple, se află în prezent în faza 2 de studii clinice. Medicamentul este un anticorp monoclonal care se poate lega în mod specific la proteina LINGO-1, care previne procesul de mielinizare și formarea de noi axoni. În consecință, dacă această proteină este „dezactivată”, mielina începe să se recupereze.
În experimentele pe animale, utilizarea noului medicament a condus la remielinizare în proporție de 90%. Pacienții cu scleroză multiplă care iau Anti-LINGO-1 au în prezent o îmbunătățire a conducerii nervului optic. Cu toate acestea, rezultatele complete ale studiilor clinice pe pacienți vor fi primite abia în 2016.