Človek in vretenčarji imajo enoten strukturni načrt in ga predstavljajo osrednji del - možgani in hrbtenjača, pa tudi periferni del - živci, ki segajo iz osrednjih organov, ki so procesi živčnih celic - nevronov.
Značilnosti nevroglijskih celic
Kot smo že povedali, je mielinska ovojnica dendritov in aksonov sestavljena iz posebnih struktur, za katere je značilna nizka stopnja prepustnosti za natrijeve in kalcijeve ione, zato imajo le potenciale mirovanja (ne morejo izvajati živčnih impulzov in opravljati električne izolacijske funkcije).
Te strukture se imenujejo Te vključujejo:
- oligodendrociti;
- fibrozni astrociti;
- celice ependima;
- plazemski astrociti.
Vsi so oblikovani iz zunanje plasti zarodka - ektoderme in imajo skupno ime - makroglija. Glijo simpatičnih, parasimpatičnih in somatskih živcev predstavljajo Schwannove celice (nevrolemociti).
Zgradba in funkcije oligodendrocitov
So del centralnega živčnega sistema in so makroglialne celice. Ker je mielin beljakovinsko-lipidna struktura, pomaga povečati hitrost vzbujanja. Celice same tvorijo električno izolacijsko plast živčnih končičev v možganih in hrbtenjači, ki nastanejo že v obdobju intrauterinega razvoja. Njihovi procesi ovijajo nevrone, pa tudi dendrite in aksone, v gube njihove zunanje plazmaleme. Izkazalo se je, da je mielin glavni električno izolacijski material, ki razmejuje živčne procese mešanih živcev.

in njihove lastnosti
Mielinsko ovojnico živcev perifernega sistema tvorijo nevrolemociti (Schwannove celice). Njihova značilnost je, da lahko tvorijo zaščitni ovoj samo enega aksona in ne morejo tvoriti procesov, kot je značilno za oligodendrocite.
Med Schwannovimi celicami na razdalji 1-2 mm so območja brez mielina, tako imenovana Ranvierjeva vozlišča. Preko njih se električni impulzi krčevito izvajajo znotraj aksona.
Lemociti so sposobni popravljati živčna vlakna in tudi opravljati.Zaradi genetskih aberacij začnejo celice membrane lemocitov nenadzorovano mitotično delitev in rast, zaradi česar se v različnih delih razvijejo tumorji - švanomi (nevrinomi). živčni sistem.
Vloga mikroglije pri uničenju mielinske strukture
Mikroglije so makrofagi, ki so sposobni fagocitoze in sposobni prepoznati različne patogene delce – antigene. Zahvaljujoč membranskim receptorjem te glialne celice proizvajajo encime - proteaze, pa tudi citokine, na primer interlevkin 1. Je mediator vnetnega procesa in imunosti.
Mielinska ovojnica, katere funkcija je izolacija aksialnega cilindra in izboljšanje prevodnosti živčnega impulza, se lahko poškoduje zaradi interlevkina. Zaradi tega je živec "gol" in stopnja vzbujanja se močno zmanjša.

Poleg tega citokini z aktivacijo receptorjev izzovejo čezmeren transport kalcijevih ionov v telo nevrona. Proteaze in fosfolipaze začnejo razgrajevati organele in procese živčnih celic, kar vodi do apoptoze - smrti te strukture.
Zruši se, razpade na delce, ki jih požrejo makrofagi. Ta pojav se imenuje ekscitotoksičnost. Povzroča degeneracijo nevronov in njihovih končičev, kar vodi do bolezni, kot sta Alzheimerjeva bolezen in Parkinsonova bolezen.
Pulpna živčna vlakna
Če so procesi nevronov - dendriti in aksoni prekriti z mielinsko ovojnico, se imenujejo kašasti in inervirajo skeletne mišice, vstopajo v somatski del perifernega živčnega sistema. Nemielinizirana vlakna tvorijo avtonomni živčni sistem in inervirajo notranje organe.

Mesasti izrastki imajo večji premer kot nemesnati in nastanejo na naslednji način: aksoni upognejo plazemsko membrano glialnih celic in tvorijo linearne mezaksone. Nato se podaljšajo in Schwannove celice se večkrat ovijejo okoli aksona in tvorijo koncentrične plasti. Citoplazma in jedro lemmocita se premakneta v področje zunanje plasti, ki se imenuje nevrilema ali Schwannova membrana.
Notranja plast lemmocita je sestavljena iz večplastnega mezoksona in se imenuje mielinska ovojnica. Njegova debelina v različnih delih živca ni enaka.
Kako popraviti mielinsko ovojnico
Glede na vlogo mikroglije v procesu demielinizacije živcev smo ugotovili, da se pod delovanjem makrofagov in nevrotransmiterjev (na primer interlevkinov) mielin uniči, kar posledično povzroči poslabšanje prehrane nevronov in motnje v prenosu. živčnih impulzov vzdolž aksonov.
Ta patologija povzroča nastanek nevrodegenerativnih pojavov: poslabšanje kognitivnih procesov, predvsem spomina in mišljenja, pojav oslabljene koordinacije gibov telesa in finih motoričnih sposobnosti.

Posledično je možna popolna invalidnost bolnika, ki nastane kot posledica avtoimunskih bolezni. Zato je vprašanje, kako obnoviti mielin, trenutno še posebej pereče. Te metode vključujejo predvsem uravnoteženo beljakovinsko-lipidno prehrano, pravilen življenjski slog in odsotnost slabih navad. V hudih primerih bolezni se zdravljenje z zdravili uporablja za obnovitev števila zrelih glialnih celic - oligodendrocitov.
Živčni sistem ljudi in vretenčarjev ima enoten strukturni načrt in ga predstavlja osrednji del - možgani in hrbtenjača, pa tudi periferni del - od centralnih organov odstopajo živci, ki so procesi živčnih celic - nevronov.
Njihova kombinacija tvori živčno tkivo, katerega glavni funkciji sta razdražljivost in prevodnost. Te lastnosti so razložene predvsem s strukturnimi značilnostmi lupin nevronov in njihovih procesov, sestavljenih iz snovi, imenovane mielin. V tem članku bomo preučili strukturo in funkcije te spojine ter ugotovili možne načine za njeno obnovitev.
Zakaj so nevrociti in njihovi procesi prekriti z mielinom
Ni naključje, da imajo dendriti in aksoni zaščitno plast, sestavljeno iz proteinsko-lipidnih kompleksov. Dejstvo je, da je kršitev biofizični proces, ki temelji na šibkih električnih impulzih. Če električni tok teče skozi žico, mora biti slednja prekrita z izolacijskim materialom, da se zmanjša disperzija električnih impulzov in prepreči zmanjšanje jakosti toka. Enake funkcije v živčnem vlaknu opravlja mielinska ovojnica. Poleg tega je podpora in daje tudi moč vlaknu.
Kemična sestava mielina
Kot večina celičnih membran ima lipoproteinsko naravo. Poleg tega je vsebnost maščobe tukaj zelo visoka - do 75%, beljakovin pa do 25%. Mielin vsebuje tudi majhno količino glikolipidov in glikoproteinov. Njegova kemična sestava se razlikuje v hrbteničnih in kranialnih živcih.
V prvem je visoka vsebnost fosfolipidov - do 45%, ostalo pa pade na holesterol in cerebroside. Demielinizacija (to je zamenjava mielina z drugimi snovmi v živčnih procesih) vodi v tako hude avtoimunske bolezni, kot je na primer multipla skleroza.
S kemijskega vidika bo ta proces videti takole: mielinska ovojnica živčnih vlaken spremeni svojo strukturo, kar se kaže predvsem v zmanjšanju odstotka lipidov glede na beljakovine. Poleg tega se zmanjša količina holesterola in poveča vsebnost vode. In vse to vodi do postopne zamenjave mielina, ki vsebuje oligodendrocite ali Schwannove celice, makrofage, astrocite in medcelično tekočino. Rezultat takšnih biokemičnih sprememb bo močno zmanjšanje sposobnosti aksonov za prevajanje vzbujanja do popolne blokade prehoda živčnih impulzov.
Značilnosti nevroglijskih celic
Kot smo že povedali, mielinsko ovojnico dendritov in aksonov tvorijo posebne strukture, za katere je značilna nizka stopnja prepustnosti za natrijeve in kalcijeve ione, zato imajo le potencial mirovanja (ne morejo prevajati živčnih impulzov in opravljati električne izolacijske funkcije). ). Te strukture imenujemo glialne celice. Tej vključujejo:
- oligodendrociti;
- fibrozni astrociti;
- ependimske celice;
- plazemski astrociti.
Vsi so oblikovani iz zunanje plasti zarodka - ektoderme in imajo skupno ime - makroglija. Glijo simpatičnega in parasimpatičnega somatskega živca predstavljajo Schwannove celice (nevrolemociti).
Zgradba in funkcije oligodendrocitov
So del centralnega živčnega sistema in so makroglialne celice. Ker je mielin beljakovinsko-lipidna struktura, pomaga povečati hitrost vzbujanja. Celice same tvorijo električno izolacijsko plast živčnih končičev v možganih in hrbtenjači, ki nastanejo že v obdobju intrauterinega razvoja. Njihovi procesi ovijajo nevrone, pa tudi dendrite in aksone, v gube njihove zunanje plazmaleme. Izkazalo se je, da je mielin glavni električno izolacijski material, ki razmejuje živčne procese mešanih živcev.
Schwannove celice in njihove lastnosti
Mielinsko ovojnico živcev perifernega sistema tvorijo nevrolemociti (Schwannove celice). Njihova značilnost je, da lahko tvorijo zaščitni ovoj samo enega aksona in ne morejo tvoriti procesov, kot je značilno za oligodendrocite. Med Schwannovimi celicami na razdalji 1-2 mm so območja brez mielina, tako imenovana Ranvierjeva vozlišča. Za njim se električni impulzi krčevito izvajajo znotraj aksona. Lemociti so sposobni popravljati živčna vlakna in opravljajo tudi trofično funkcijo. Zaradi genetskih aberacij se celice ovojnice lemocitov začnejo nenadzorovano mitotično deliti in rasti, zaradi česar se v različnih delih živčnega sistema razvijejo tumorji, švanomi (nevrinomi).
Vloga mikroglije pri uničenju mielinske strukture
Mikroglije so makrofagi, ki so sposobni fagocitoze in so sposobni prepoznati različne patogene delce – antigene. Zahvaljujoč membranskim receptorjem te glialne celice proizvajajo encime - proteaze, pa tudi citokine, na primer interlevkin 1. Je mediator vnetnega procesa in imunosti. Interlevkin lahko poškoduje mielinsko ovojnico, katere funkcija je izolacija aksialnega cilindra in izboljšanje prevodnosti živčnih impulzov. Zaradi tega je živec "izpostavljen" in stopnja prevodnosti vzbujanja se močno zmanjša.
Poleg tega citokini z aktivacijo receptorjev izzovejo čezmeren transport kalcijevih ionov v telo nevrona. Proteaze in fosfolipaze začnejo razgrajevati organele in procese živčnih celic, kar vodi do apoptoze - smrti te strukture. Zruši se, razpade na delce, ki jih požrejo makrofagi. Ta pojav se imenuje ekscitotoksičnost. Povzroča degeneracijo nevronov in njihovih končičev, kar vodi do bolezni, kot sta Alzheimerjeva bolezen in Parkinsonova bolezen.
Pulpna živčna vlakna
Če so procesi nevronov - dendriti in aksoni prekriti z mielinsko ovojnico, se imenujejo kašasti in inervirajo skeletne mišice, vstopajo v somatski del perifernega živčnega sistema. Nemielinizirana vlakna tvorijo avtonomni živčni sistem in inervirajo notranje organe.
Kašasti procesi imajo večji premer kot nepulmonalni procesi in nastanejo na naslednji način: aksoni upognejo plazemsko membrano glialnih celic in tvorijo linearne mezaksone. Nato se povečajo in Schwannove celice se večkrat ovijejo okoli aksona in tvorijo koncentrične plasti. Citoplazma in jedro lemmocita se premakneta v področje zunanje plasti, ki se imenuje nevrilema ali Schwannova membrana. Notranja plast lemmocita je sestavljena iz večplastnega mezoksona in se imenuje mielinska ovojnica. Njegova debelina v različnih delih živca ni enaka.
Kako popraviti mielinsko ovojnico
Glede na vlogo mikroglije v procesu demielinizacije živcev smo ugotovili, da se pod delovanjem makrofagov in nevrotransmiterjev (na primer interlevkinov) mielin uniči, kar posledično vodi do poslabšanja prehrane nevronov in kršitve prenosa. živčnih impulzov vzdolž aksonov. Ta patologija povzroča nastanek nevrodegenerativnih pojavov: poslabšanje kognitivnih procesov, predvsem spomina in mišljenja, pojav oslabljene koordinacije gibov telesa in finih motoričnih sposobnosti.
Posledično je možna popolna invalidnost bolnika, ki nastane kot posledica avtoimunskih bolezni. Zato je vprašanje, kako obnoviti mielin, trenutno še posebej pereče. Te metode vključujejo predvsem uravnoteženo beljakovinsko-lipidno prehrano, pravilen življenjski slog in odsotnost slabih navad. V hudih primerih bolezni se zdravljenje z zdravili uporablja za obnovitev števila zrelih glialnih celic - oligodendrocitov.
Datum objave: 26.05.17Centralni živčni sistem (CNS) je enoten mehanizem, ki je odgovoren za zaznavanje okoliškega sveta in reflekse ter za nadzor sistema notranjih organov in tkiv. Zadnjo točko opravlja periferni del centralnega živčnega sistema s pomočjo posebnih celic, imenovanih nevroni. Iz njih je sestavljeno živčno tkivo, ki služi za prenos impulzov.
Procesi, ki prihajajo iz telesa nevrona, so obdani z zaščitno plastjo, ki hrani živčna vlakna in pospešuje prenos impulzov, takšno zaščito pa imenujemo mielinska ovojnica. Vsak signal, ki se prenaša skozi živčna vlakna, je podoben izpustu toka in njihova zunanja plast ne dopušča, da bi se njegova moč zmanjšala.
Če je mielinska ovojnica poškodovana, potem je popolna zaznava v tem delu telesa izgubljena, vendar celica lahko preživi in poškodba se čez čas zaceli. Z dovolj resnimi poškodbami bodo potrebna zdravila za obnovo živčnih vlaken, kot so Milgamma, Copaxone in drugi. V nasprotnem primeru bo živec sčasoma odmrl in zaznavanje se bo zmanjšalo. Bolezni, za katere je značilna ta težava, vključujejo radikulopatijo, polinevropatijo itd., vendar zdravniki menijo, da je multipla skleroza (MS) najnevarnejši patološki proces. Kljub čudnemu imenu bolezen nima nobene zveze z neposredno definicijo teh besed in v prevodu pomeni "več brazgotin". Nastanejo na mielinski ovojnici v hrbtenjači in možganih zaradi imunske odpovedi, zato je MS avtoimunska bolezen. Namesto živčnih vlaken se na mestu žarišča pojavi brazgotina, sestavljena iz vezivnega tkiva, skozi katerega impulz ne more več pravilno prehajati.
Ali je mogoče nekako obnoviti poškodovano živčno tkivo ali bo za vedno ostalo v pohabljenem stanju? Zdravniki še vedno ne morejo natančno odgovoriti in še niso našli popolnega zdravila za obnovitev občutljivosti živčnih končičev. Namesto tega obstajajo različna zdravila, ki lahko zmanjšajo proces demielinizacije, izboljšajo prehrano poškodovanih območij in aktivirajo regeneracijo mielinske ovojnice.
Milgamma je nevroprotektor za obnovo metabolizma v celicah, kar vam omogoča, da upočasnite proces uničenja mielina in začnete njegovo regeneracijo. Zdravilo temelji na vitaminih skupine B, in sicer:
- Tiamin (B1). Nujen je za absorpcijo sladkorja v telesu in energijo. Pri akutnem pomanjkanju tiamina pri osebi pride do motenj spanja in poslabšanja spomina. Postane živčen in včasih depresiven, kot pri depresiji. V nekaterih primerih se pojavijo simptomi parestezije (kurja koža, zmanjšana občutljivost in mravljinčenje v konicah prstov);
- piridoksin (B6). Ta vitamin ima pomembno vlogo pri nastajanju aminokislin, pa tudi nekaterih hormonov (dopamin, serotonin itd.). Kljub redkim primerom pomanjkanja piridoksina v telesu je zaradi njegovega pomanjkanja možno zmanjšanje duševnih sposobnosti in oslabitev imunske obrambe;
- cianokobalamin (B12). Služi za izboljšanje prevodnosti živčnih vlaken, kar ima za posledico izboljšano občutljivost, pa tudi za izboljšanje sinteze krvi. S pomanjkanjem cianokobalamina se pri človeku razvijejo halucinacije, demenca (demenca), pride do motenj srčnega ritma in parestezije.
Zahvaljujoč tej sestavi je Milgama sposobna ustaviti oksidacijo celic s prostimi radikali (reaktivnimi snovmi), kar bo vplivalo na obnovitev občutljivosti tkiv in živčnih končičev. Po poteku jemanja tablet se zmanjšajo simptomi in izboljša splošno stanje, zdravilo pa je treba jemati v dveh fazah. V prvem boste morali narediti vsaj 10 injekcij, nato pa preiti na tablete (Milgamma compositum) in jih jemati 3-krat na dan 1,5 meseca.

Stafaglabrin sulfat se že dolgo uporablja za obnovitev občutljivosti tkiv in samih živčnih vlaken. Rastlina, iz korenin katere pridobivajo to zdravilo, raste samo v subtropskem in tropskem podnebju, na primer na Japonskem, v Indiji in Burmi, in se imenuje Stephania smooth. Obstajajo primeri pridobivanja stafaglabrin sulfata v laboratoriju. Morda je to posledica dejstva, da se stephania smooth lahko goji kot suspenzijska kultura, to je v suspendiranem položaju v steklenih bučkah s tekočino. Samo po sebi je zdravilo sulfatna sol, ki ima visoko tališče (več kot 240 ° C). Nanaša se na alkaloid (spojina, ki vsebuje dušik) stefarin, ki velja za osnovo za proaporfin.
Stefaglabrin sulfat služi za zmanjšanje aktivnosti encimov iz razreda hidrolaz (holinesteraze) in za izboljšanje tonusa gladkih mišic, ki so prisotne v stenah krvnih žil, organov (znotraj votlih) in bezgavk. Znano je tudi, da je zdravilo rahlo strupeno in lahko zniža krvni tlak. V starih časih so zdravilo uporabljali kot antiholinesterazno sredstvo, potem pa so znanstveniki prišli do zaključka, da je stefaglabrin sulfat zaviralec aktivnosti rasti vezivnega tkiva. Iz tega se izkaže, da zamuja njegov razvoj in na živčnih vlaknih ne nastanejo brazgotine. Zato se je zdravilo začelo aktivno uporabljati za poškodbe PNS.
Med raziskavo so strokovnjaki lahko videli rast Schwannovih celic, ki proizvajajo mielin v perifernem živčnem sistemu. Ta pojav pomeni, da se pri bolniku pod vplivom zdravila opazno izboljša prevodnost impulza vzdolž aksona, saj se okoli njega ponovno začne tvoriti mielinska ovojnica. Odkar so bili rezultati pridobljeni, je zdravilo postalo upanje za mnoge ljudi z diagnozo neozdravljivih demielinizirajočih patologij.

Problema avtoimunske patologije ne bo mogoče rešiti samo z obnovo živčnih vlaken. Dejansko, ne glede na to, koliko žarišč poškodb je treba odpraviti, se bo težava vrnila, saj imunski sistem reagira na mielin kot na tuje telo in ga uniči. Do danes je nemogoče odpraviti tak patološki proces, vendar se ne moremo več spraševati, ali so živčna vlakna obnovljena ali ne. Ljudem je prepuščeno, da vzdržujejo svoje stanje z zatiranjem imunskega sistema in uporabo zdravil, kot je stefaglabrin sulfat, da ohranijo svoje zdravje.
Zdravilo se lahko uporablja samo parenteralno, to je s črevesjem, na primer z injekcijo. Odmerjanje v tem primeru ne sme preseči 7-8 ml 0,25% raztopine na dan za 2 injekciji. Sodeč po času, se mielinska ovojnica in živčni končiči običajno do neke mere obnovijo po 20 dneh, nato pa potrebujete odmor in lahko razumete, kako dolgo bo trajalo, potem ko se o tem seznanite z zdravnikom. Najboljši rezultat je po mnenju zdravnikov mogoče doseči na račun majhnih odmerkov, saj se stranski učinki razvijejo veliko manj pogosto, učinkovitost zdravljenja pa se poveča.
V laboratorijskih pogojih, v času poskusov na podganah, je bilo ugotovljeno, da je s koncentracijo zdravila Stefaglabrin sulfat 0,1-1 mg / kg zdravljenje hitrejše kot brez njega. Potek terapije se je končal prej v primerjavi z živalmi, ki tega zdravila niso jemale. Po 2-3 mesecih so bila živčna vlakna pri glodavcih skoraj popolnoma obnovljena, impulz pa se je brez odlašanja prenašal po živcu. Pri poskusnih osebah, ki so bile zdravljene brez tega zdravila, je okrevanje trajalo približno šest mesecev in vsi živčni končiči se niso vrnili v normalno stanje.
Copaxone

Zdravila za multiplo sklerozo ni, obstajajo pa zdravila, ki lahko zmanjšajo vpliv imunskega sistema na mielinsko ovojnico, in Copaxone je eno izmed njih. Bistvo avtoimunskih bolezni je, da imunski sistem uniči mielin, ki se nahaja na živčnih vlaknih. Zaradi tega se prevodnost impulzov poslabša, Copaxone pa lahko sam sebi spremeni cilj obrambnega sistema telesa. Živčna vlakna ostanejo nedotaknjena, če pa so celice telesa že prevzele erozijo mielinskega ovoja, jih bo zdravilo lahko potisnilo nazaj. Ta pojav se pojavi zaradi dejstva, da je zdravilo po strukturi zelo podobno mielinu, zato imunski sistem preusmeri pozornost nanj.
Zdravilo ne more samo prevzeti napada obrambnega sistema telesa, temveč tudi proizvaja posebne celice imunskega sistema za zmanjšanje intenzivnosti bolezni, ki se imenujejo Th2-limfociti. Mehanizem njihovega vpliva in nastanka še ni dovolj raziskan, vendar obstajajo različne teorije. Med strokovnjaki obstaja mnenje, da dendritične celice povrhnjice sodelujejo pri sintezi Th2-limfocitov.
Razviti supresorski (mutirani) limfociti, ki vstopijo v kri, hitro prodrejo v del živčnega sistema, kjer se nahaja žarišče vnetja. Tu limfociti Th2 zaradi vpliva mielina proizvajajo citokine, to je protivnetne molekule. Začnejo postopoma lajšati vnetje v tem delu možganov in s tem izboljšati občutljivost živčnih končičev.
Korist zdravila ni samo za zdravljenje same bolezni, ampak tudi za same živčne celice, saj je Copaxone nevroprotektor. Zaščitni učinek se kaže v stimulaciji rasti možganskih celic in izboljšanju metabolizma lipidov. Mielinska ovojnica je v glavnem sestavljena iz lipidov in pri mnogih patoloških procesih, povezanih s poškodbo živčnih vlaken, pride do njihove oksidacije, zato pride do poškodbe mielina. Zdravilo Copaxone lahko odpravi to težavo, saj poveča naravni antioksidant v telesu (sečno kislino). Zakaj se raven sečne kisline dvigne, ni znano, vendar je bilo to dejstvo dokazano s številnimi poskusi.
Zdravilo služi za zaščito živčnih celic ter zmanjša resnost in pogostost poslabšanj. Lahko se kombinira z zdravili Stefaglabrin sulfat in Milgamma.
Mielinska ovojnica se bo začela obnavljati zaradi povečane rasti Schwannovih celic, Milgamma pa bo izboljšala znotrajcelično presnovo in okrepila učinek obeh zdravil. Strogo prepovedano jih je uporabljati samostojno ali samostojno spreminjati odmerek.
Ali je mogoče obnoviti živčne celice in koliko časa bo trajalo, lahko odgovori le specialist, ki se osredotoča na rezultate pregleda. Prepovedano je samostojno jemati kakršna koli zdravila za izboljšanje občutljivosti tkiv, saj ima večina hormonsko osnovo, kar pomeni, da jih telo težko prenaša.
ŽIVČNA VLAKNA
Živčna vlakna so procesi nevronov, prekriti z glialnimi ovojnicami. Obstajata dve vrsti živčnih vlaken - nemielinizirana in mielinizirana. Obe vrsti sta sestavljeni iz centralno ležečega procesa nevrona (aksialni cilinder), obdanega z ovojnico celic oligodendroglije (v PNS jih imenujemo lemociti ali Schwannove celice).
nemielinizirana živčna vlakna pri odraslih se nahajajo predvsem v avtonomnem živčnem sistemu in je značilna relativno nizka hitrost prevodnosti živčnih impulzov (0.5-2 gospa). Nastanejo s potopitvijo aksialnega cilindra (aksona) v citoplazmo lemocitov, ki se nahajajo v obliki niti. V tem primeru se plazmolema lemocita upogne, obdaja akson in tvori podvojitev - mezakson (sl. 14-7). Pogosto je lahko v citoplazmi enega lemocita do 10-20 osni cilindri. Takšno vlakno spominja na električni kabel in se zato imenuje kabelsko vlakno. Površina vlaken je prekrita z bazalno membrano. V osrednjem živčevju, še posebej med njegovim razvojem, so opisana nemielinizirana vlakna, sestavljena iz "golega" aksona, brez ovoja lemocitov.
riž. 14-7. Tvorba mieliniziranih (1-3) in nemieliniziranih (4) živčnih vlaken v perifernem živčnem sistemu. Živčno vlakno nastane s potopitvijo aksona (A) živčne celice v citoplazmo lemocita (LC). Ko nastane mielinsko vlakno, se podvojitev LC plazmoleme - mezakson (MA) - navije okoli A in tvori zavoje mielinske ovojnice (MO). V vlaknu brez mielina, prikazanem na sliki, je več A potopljenih v citoplazmo LC (vlakna tipa kabla). Jaz sem jedro LC.

mielinizirana živčna vlakna najdemo v CNS in PNS in zanje je značilna visoka hitrost prevodnosti živčnih impulzov (5-120 gospa). Mielinizirana vlakna so običajno debelejša od nemieliniziranih in vsebujejo aksialne valje večjega premera. V mielinskem vlaknu je aksialni valj neposredno obdan s posebno mielinsko ovojnico, okoli katere je tanka plast, ki vključuje citoplazmo in jedro lemocita - nevrolemo (sl. 14-8 in 14-9). Zunaj je vlakno prekrito tudi z bazalno membrano. Mielinska ovojnica vsebuje visoke koncentracije lipidov in je intenzivno obarvana z osmično kislino, pod svetlobnim mikroskopom je videti kot homogena plast, pod elektronskim mikroskopom pa je ugotovljeno, da nastane kot posledica zlitja številnih (do 300) membranske tuljave (plošče).
riž. 14-8. Struktura mieliniziranega živčnega vlakna. Mielinsko vlakno je sestavljeno iz aksialnega cilindra ali aksona (A), ki je neposredno obdan z mielinsko ovojnico (MO) in nevrolemo (NL), vključno s citoplazmo (CL) in lemocitnim jedrom (NL). Zunaj je vlakno prekrito z bazalno membrano (BM). Področja MO, v katerih so ohranjene vrzeli med mielinskimi zavoji, napolnjene s CL in zato niso obarvane z osmijem, imajo obliko mielinskih zarez (MN).
Nastanek mielinske ovojnice nastane med interakcijo aksialnega cilindra in celic oligodendroglije z nekaterimi razlikami v PNS in CNS.
Tvorba mielinske ovojnice v PNS : potopitev aksialnega cilindra v lemmocit spremlja tvorba dolgega mesaksona, ki se začne vrteti okoli aksona in tvori prve ohlapno razporejene zavoje mielinske ovojnice (glej sliko 1). 14-7). Ko se število zavojev (plošč) v procesu zorenja mielina povečuje, se razporejajo vedno bolj na gosto in se delno združijo; vrzeli med njimi, napolnjene s citoplazmo lemocita, so ohranjene le na ločenih območjih, ki niso obarvana z osmijem - mielinske zareze (Schmidt-Lanterman). Med tvorbo mielinskega ovoja sta citoplazma in jedro lemmocita potisnjena na obrobje vlakna, kar tvori nevrolemo. Mielinska ovojnica ima nekontinuiran potek vzdolž dolžine vlakna.

riž. 14-9. Ultrastrukturna organizacija mieliniziranega živčnega vlakna. Okoli aksona (A) so zvitki mielinske ovojnice (MMO), zunaj prekrite z nevrolemo, ki vključuje citoplazmo (CL) in jedro lemocita (NL). Vlakno je na zunanji strani obdano z bazalno membrano (BM). CL poleg nevroleme tvori notranji list (IL), ki meji neposredno na A (ki se nahaja med njim in SMO), vsebuje pa ga tudi območje, ki ustreza meji sosednjih lemocitov - nodalno prestrezanje (NC), kjer je mielinska ovojnica odsotna, in na območjih ohlapnega zlaganja WMO - mielinske zareze (MN).
Nodalna prestrezanja (Ranvier)- območja v območju meje sosednjih lemmocitov, kjer je mielinska ovojnica odsotna, akson pa je prekrit le z interdigitacijskimi procesi sosednjih lemmocitov (glej sliko 14-9). Vozlišča se ponavljajo vzdolž poteka mielinskega vlakna z intervalom, ki je v povprečju enak 1-2 mm. V območju nodalnega vozla se akson pogosto razširi, njegova plazmolema pa vsebuje številne natrijeve kanale (ki jih zunaj vozlišč pod mielinsko ovojnico ni).
Širjenje depolarizacije v mielinskih vlaknih izvaja se v skokih iz prestrezanja v prestrezanje (saltatorno). Depolarizacijo v območju enega nodalnega stičišča spremlja hitro pasivno širjenje vzdolž aksona do naslednjega stičišča (ker je uhajanje toka v internodalni regiji minimalno zaradi visokih izolacijskih lastnosti mielina). V območju naslednjega prestrezanja impulz povzroči vklop obstoječih ionskih kanalov in pojavi se novo območje lokalne depolarizacije itd.
Tvorba mielinske ovojnice v CNS: aksialni valj se ne potopi v citoplazmo oligodendrocita, ampak je prekrit s svojim ploščatim procesom, ki se nato vrti okoli njega, izgubi citoplazmo in njegove tuljave se spremenijo v plošče mielinskega ovoja

komolci (slika 14-10). V nasprotju s Schwannovimi celicami lahko en oligodendrocit CNS s svojimi procesi sodeluje pri mielinizaciji številnih (do 40-50) živčnih vlaken. Mesta aksonov v območju Ranvierjevih vozlišč v CNS niso pokrita s citoplazmo oligodendrocitov.
riž. 14-10. Tvorba mielinskih vlaken z oligodendrociti v CNS. 1 - akson (A) nevrona je prekrit s ploščatim procesom (PO) oligodendrocita (ODC), katerega tuljave se spremenijo v plošče mielinske ovojnice (MO). 2 - en ODC s svojimi procesi lahko sodeluje pri mielinizaciji številnih A. Območja A v območju nodalnih prestreznikov (NC) niso pokrita s citoplazmo ODC.
Kršitev tvorbe in poškodbe oblikovanega mielina so osnova številnih resnih bolezni živčnega sistema. Mielin v CŽS je lahko tarča avtoimunskih poškodb T-limfociti in makrofage z njegovim uničenjem (demielinizacija). Ta proces se aktivno nadaljuje pri multipli sklerozi, resni bolezni nejasne (verjetno virusne) narave, povezane z motnjami različnih funkcij, razvojem paralize in izgubo občutljivosti. Narava nevroloških motenj je določena s topografijo in velikostjo poškodovanih območij. Pri nekaterih presnovnih motnjah pride do motenj tvorbe mielina - levkodistrofije, ki se v otroštvu kaže s hudimi poškodbami živčnega sistema.
Razvrstitev živčnih vlaken
Razvrstitev živčnih vlaken temelji na razlikah v njihovi zgradbi in delovanju (hitrost živčnih impulzov). Obstajajo tri glavne vrste živčnih vlaken:
1. Vlakna tipa A - debel, mieliniziran, z daleč oddaljenimi vozlišči. Vodite impulze pri visoki hitrosti
(15-120 m/s); razdeljen na 4 podtipe (α, β, γ, δ) z padajočim premerom in hitrostjo prevodnosti impulza.
2. Vlakna tipa B - srednje debeline, mielinska, manjši premer,
kot vlakna tipa A, s tanjšo mielinsko ovojnico in manjšo hitrostjo prevajanja živčnih impulzov (5-15 m/s).
3. Vlakna tipa C - tanka, nemielinizirana, izvajajo impulze z relativno nizko hitrostjo(0,5-2 m/s).
Regeneracija živčnih vlaken v PNS vključuje naravno odvijajoče se kompleksno zaporedje procesov, med katerimi nevronski proces aktivno sodeluje z glialnimi celicami. Dejanska regeneracija vlaken sledi nizu reaktivnih sprememb, ki jih povzroči njihova poškodba.
Reaktivne spremembe živčnega vlakna po njegovem prerezu. V 1. tednu po prerezu živčnega vlakna se razvije ascendentna degeneracija proksimalnega (telesu nevrona najbližjega) dela aksona, na koncu katerega nastane podaljšek (retrakcijska bučka). Mielinska ovojnica na območju poškodbe razpade, telo nevrona nabrekne, jedro se premakne na obrobje, kromatofilna snov se raztopi (sl. 14-11).
V distalnem delu vlakna po njegovem prerezu opazimo descendentno degeneracijo s popolnim uničenjem aksona, razgradnjo mielina in kasnejšo fagocitozo detritusa s strani makrofagov in glije.
Strukturne transformacije med regeneracijo živčnega vlakna. Po 4-6 tednih. struktura in funkcija nevrona se obnovita, iz retrakcijske bučke začnejo rasti tanke veje (rastni stožci) v smeri distalnega dela vlakna. Schwannove celice v proksimalnem delu vlakna proliferirajo in tvorijo trakove (Büngner) vzporedno s potekom vlakna. V distalnem delu vlakna vztrajajo tudi Schwannove celice, ki se mitotično delijo in tvorijo trakove, ki se povezujejo s podobnimi tvorbami v proksimalnem delu.
Regeneracijski akson raste v distalni smeri s hitrostjo 3-4 mm/dan. po Büngnerjevih trakovih, ki imajo nosilno in usmerjevalno vlogo; Schwannove celice tvorijo novo mielinsko ovojnico. Kolaterale in terminali aksonov se obnovijo v nekaj mesecih.

riž. 14-11. Regeneracija mieliniziranega živčnega vlakna (po R.Krstic, 1985, s spremembami). 1 - po prerezu živčnega vlakna se proksimalni del aksona (A) podvrže naraščajoči degeneraciji, mielinska ovojnica (MO) v območju poškodbe razpade, perikarion (PC) nevrona nabrekne, jedro se premakne na periferijo razpade kromatofilna snov (CS) (2). Distalni del, povezan z inerviranim organom (v danem primeru skeletno mišico), je podvržen degeneraciji navzdol s popolnim uničenjem A, razpadom MO in fagocitozo detritusa s strani makrofagov (MF) in glije. Lemociti (LC) vztrajajo in se mitotično delijo ter tvorijo niti - Büngnerjeve trakove (LB), ki se povezujejo s podobnimi tvorbami v proksimalnem delu vlakna (tanke puščice). Po 4-6 tednih se struktura in funkcija nevrona obnovita, tanke veje rastejo distalno od proksimalnega dela A (krepka puščica), rastejo vzdolž LB (3). Zaradi regeneracije živčnega vlakna se ponovno vzpostavi povezava s tarčnim organom (mišico) in nazaduje njegova atrofija, ki jo povzroča okvara inervacije (4). V primeru ovire (P) na poti regeneracije A (npr. brazgotina vezivnega tkiva) se komponente živčnega vlakna
tvorijo travmatski nevrom (TN), ki je sestavljen iz rastočih vej A in LC (5).
pogoji regeneracije so: brez poškodb telesa nevrona, majhna razdalja med deli živčnega vlakna, odsotnost vezivnega tkiva, ki lahko zapolni vrzel med deli vlakna. Ko pride do ovire na poti obnavljajočega se aksona, nastane travmatični (amputacijski) nevrom, ki je sestavljen iz rastočega aksona in Schwannovih celic, ki so spajkane v vezivno tkivo.
V CŽS ni regeneracije živčnih vlaken : čeprav imajo nevroni CNS sposobnost obnoviti svoje procese, se to ne zgodi, očitno zaradi škodljivega vpliva mikrookolja. Po poškodbi nevrona mikroglija, astrociti in hematogeni makrofagi fagocitirajo detritus na območju uničenega vlakna, proliferirajoči astrociti pa na njegovem mestu tvorijo gosto glialno brazgotino.
ŽIVČNI KONČI
Živčni končiči- končne naprave živčnih vlaken. Glede na funkcijo jih delimo v tri skupine:
1) internevronski stiki (sinapse)- zagotavljajo funkcionalno povezavo med nevroni;
2) eferentne (efektorske) končnice- prenašajo signale iz živčnega sistema v izvršilne organe (mišice, žleze), so prisotni na aksonih;
3) receptorski (občutljivi) končičizaznavajo draženja iz zunanjega in notranjega okolja, so prisotni na dendritih.
NOTRANJEVRNSKI STIKI (SINAPSA)
Internevronski stiki (sinapse) delimo na električne in kemične.
električne sinapse redko v CŽS sesalcev; imajo strukturo vrzelnih stikov, v katerih so membrane sinaptično povezanih celic (pred- in postsinaptičnih) ločene z 2 nm široko režo, ki jo predrejo koneksoni. Slednje so cevi, ki jih tvorijo beljakovinske molekule in služijo kot vodni kanali, skozi katere se lahko majhne molekule in ioni prenašajo iz ene celice v drugo.

drugo (glejte 3. poglavje). Ko akcijski potencial, ki se širi po membrani ene celice, doseže režni spoj, električni tok pasivno teče skozi režo iz ene celice v drugo. Impulz se lahko prenaša v obe smeri in skoraj brez zakasnitve.
Kemične sinapse- najpogostejši tip pri sesalcih. Njihovo delovanje temelji na pretvorbi električnega signala v kemični signal, ki se nato pretvori nazaj v električnega. Kemična sinapsa je sestavljena iz treh komponent: presinaptičnega dela, postsinaptičnega dela in sinaptične špranje (slika 14-12). V presinaptičnem delu je (nevro)transmiter, ki se pod vplivom živčnega impulza sprosti v sinaptično špranjo in z vezavo na receptorje v postsinaptičnem delu povzroči spremembo ionske prepustnosti njene membrane, kar vodi do depolarizacija (v ekscitatornih sinapsah) ali hiperpolarizacija (v inhibitornih sinapsah). Kemične sinapse se od električnih razlikujejo po enostranskem prevajanju impulzov, zakasnitvi njihovega prenosa (sinaptična zakasnitev 0,2–0,5 ms) in zagotavljanju tako vzbujanja kot inhibicije postsinaptičnih nevronov.
riž. 14-12. Struktura kemične sinapse. Presinaptični del (PRSP) ima obliko končnega gumba (CB) in vključuje: sinaptične vezikle (SP), mitohondrije (MTX), nevrotubule (NT), nevrofilamente (NF), presinaptično membrano (PRSM) s presinaptično zbijanjem (PRSU). ). Postsinaptični del (PSCH) vključuje postsinaptično membrano (POSM) s postsinaptično zbijanjem (POSU). Sinaptična špranja (SC) vsebuje intrasinaptične filamente (ISF).
1. presinaptični del tvori akson vzdolž svojega poteka (mimoidoča sinapsa) ali pa je podaljšan končni del aksona (terminalni zametek). Vsebuje mitohondrije, aER, nevrofilamente, nevrotubule in sinaptične vezikle s premerom 20-65 nm, ki vsebujejo nevrotransmiter. Oblika in narava vsebine veziklov sta odvisni od nevrotransmiterjev v njih. Okrogli lahki vezikli običajno vsebujejo acetilholin, vezikli s kompaktnim gostim središčem - norepinefrin, veliki gosti vezikli z lahkim submembranskim robom - peptidi. Nevrotransmiterji nastanejo v telesu nevrona in se z mehanizmom hitrega transporta prenesejo do končičev aksonov, kjer se odložijo. Delno se sinaptični vezikli tvorijo v sami sinapsi tako, da se odcepijo od cistern aER. Na notranji strani plazmoleme, obrnjeni proti sinaptični špranje (presinaptična membrana), je presinaptično tesnilo, ki ga tvori fibrilarna heksagonalna proteinska mreža, katere celice prispevajo k enakomerni porazdelitvi sinaptičnih veziklov po površini membrane.
2. postsinaptični del Predstavlja ga postsinaptična membrana, ki vsebuje posebne komplekse integralnih proteinov - sinaptičnih receptorjev, ki se vežejo na nevrotransmiter. Membrana je zadebeljena zaradi kopičenja gostega nitastega proteinskega materiala pod njo (postsinaptično zbijanje). Glede na to, ali je postsinaptični del internevronske sinapse dendrit, telo nevrona ali (redkeje) njegov akson, sinapse delimo na aksodendritične, aksosomatske in aksoaksonske.
3. sinaptična špranjaŠirina 20-30 nm včasih vsebuje prečne glikoproteinske intrasinaptične filamente debeline 5 nm, ki so elementi specializiranega glikokaliksa, ki zagotavljajo adhezivne vezi pre- in postsinatičnega dela ter usmerjeno difuzijo mediatorja.
Mehanizem prenosa živčnega impulza v kemični sinapsi. Pod vplivom živčnega impulza se aktivirajo napetostno odvisni kalcijevi kanali presinaptične membrane; Sa 2+ hiti do aksona, se membrane sinaptičnih veziklov ob prisotnosti Ca2+ spojijo s presinaptično membrano, njihova vsebina (mediator) pa se po mehanizmu eksocitoze sprosti v sinaptično špranjo. Z delovanjem na receptorje postsinaptične membrane povzroči mediator bodisi njeno depolarizacijo, nastanek postsinaptičnega akcijskega potenciala in nastanek živčnega impulza bodisi njeno hiperpigmentacijo.
polarizacijo, kar povzroči zaviralni odziv. Ekscitatorna mediatorja sta na primer acetilholin in glutamat, medtem ko inhibicijo posredujeta GABA in glicin.
Po prekinitvi interakcije mediatorja z receptorji postsinaptične membrane večino njegove endocitoze zajame presinaptični del, manjši del pa se razprši v prostoru in zajamejo okoliške glialne celice. Nekatere mediatorje (na primer acetilholin) encimi razgradijo na komponente, ki jih nato ujame presinaptični del. Membrane sinaptičnih veziklov, vdelane v presinaptično membrano, se nadalje vključijo v vezikle, obložene z endociti, in ponovno uporabijo za tvorbo novih sinaptičnih veziklov.
V odsotnosti živčnega impulza presinaptični del sprosti posamezne majhne porcije mediatorja, kar povzroči spontane miniaturne potenciale v postsinaptični membrani.
EFERENTNI (EFEKTORSKI) ŽIVČNI KONČI
Eferentni (efektorski) živčni končiči Glede na naravo inerviranega organa jih delimo na motorične in sekretorne. Motorni končiči se nahajajo v progastih in gladkih mišicah, sekretorni - v žlezah.
Živčnomišični konec (živčnomišični spoj, motorični plak) - motorični konec aksona motoričnega nevrona na vlaknih progastih somatskih mišic - sestoji iz terminalne veje aksona, ki tvori presinaptični del, specializiranega področja na mišičnem vlaknu, ki ustreza postsinaptičnemu delu in sinaptična špranja, ki ju ločuje (sl. 14-13).
V velikih mišicah, ki razvijejo znatno moč, en akson, ki se razveja, inervira veliko število (stotine in tisoče) mišičnih vlaken. Nasprotno, v majhnih mišicah, ki izvajajo fine gibe (na primer zunanje mišice očesa), je vsako vlakno ali njihova majhna skupina inervirana z ločenim aksonom. En motorični nevron skupaj z mišičnimi vlakni, ki jih inervira, tvori motorično enoto.
presinaptični del. V bližini mišičnega vlakna akson izgubi mielinsko ovojnico in povzroči več vej, ki
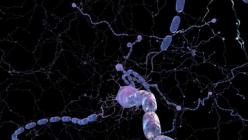
Multipla skleroza je še en dokaz o nepopolnosti našega imunskega sistema, ki včasih »ponori« in začne napadati ne zunanjega »sovražnika«, ampak tkiva svojega telesa. Pri tej bolezni celice imunskega sistema uničijo mielinsko ovojnico živčnih vlaken, ki nastane med razvojem telesa iz določene vrste glialnih celic – »službenih« celic živčnega sistema. Mielinska ovojnica pokriva aksone – dolge izrastke nevrona, ki delujejo kot »žice«, po katerih potuje živčni impulz. Sam plašč služi kot električna izolacija in zaradi njegovega uničenja se prehod impulza vzdolž živčnega vlakna upočasni za 5-10 krat.
Na fotografiji so vidne kopičenja makrofagov (rjave barve) po obodu plakov. Makrofage pritegne lezija in jih aktivirajo druge celice imunskega sistema - T-limfociti. Aktivirani makrofagi fagocitirajo (»pojedo«) odmirajoči mielin, poleg tega pa tudi sami prispevajo k njegovi poškodbi, pri čemer proizvajajo proteaze, provnetne molekule in reaktivne kisikove spojine. (Imunohistokemija, makrofagni marker - CD68).
Običajno celice imunskega sistema, tako kot druge krvne celice, ne morejo prodreti neposredno v živčno tkivo - ne dovoljuje jim tako imenovana krvno-možganska pregrada. Pri multipli sklerozi pa ta ovira postane prehodna: »nori« limfociti dobijo dostop do nevronov in njihovih aksonov, kjer začnejo napadati molekule mielina, ki so zapletena večplastna proteinsko-lipidna struktura. To sproži kaskado molekularnih dogodkov, ki vodijo do uničenja mielina in včasih samih aksonov.
Uničenje mielina spremlja razvoj vnetja in skleroze prizadetega območja, tj. nastanek vezivnotkivne brazgotine v obliki plaka, ki nadomesti mielinsko ovojnico. Skladno s tem je na tem področju oslabljena prevodna funkcija aksona. Plaki se nahajajo difuzno, razpršeni po živčnem sistemu. S to razporeditvijo lezij je povezano samo ime bolezni - »multipla« skleroza, ki nima nič skupnega z navadno odsotnostjo (tisto, o kateri včasih govorimo v vsakdanjem življenju - »imam popolnoma sklerozo, Spet sem vse pozabil«).
Simptomi multiple skleroze so različni in odvisni od tega, kateri živci so prizadeti. Med njimi so paraliza, težave z ravnotežjem, kognitivne motnje, spremembe v delovanju čutil (pri četrtini bolnikov se razvoj bolezni začne z okvaro vida zaradi optičnega nevritisa).
Sodobno zdravljenje multiple skleroze pušča veliko želenega.
Učinkovitega zdravljenja še ni, še posebej, ker vzroki za to bolezen še vedno niso znani, obstajajo le podatki o morebitnem vplivu okolja in genetski predispoziciji. Za zdravljenje, poleg simptomatske terapije, ki lahko lajša bolečine in zmanjša mišične krče, se uporabljajo glukokortikoidni pripravki za zmanjšanje vnetja, pa tudi imunomodulatorji in imunosupresivi, namenjeni zatiranju "slabe" aktivnosti imunskega sistema. Vsa ta zdravila lahko upočasnijo razvoj bolezni in zmanjšajo pogostost poslabšanj, vendar bolnika ne ozdravijo v celoti. Ni zdravil, ki bi lahko popravila že poškodovan mielin.
Vendar pa se lahko kmalu pojavi takšno zdravilo, namenjeno predvsem obnavljanju mielina in ne le upočasnitvi patološkega procesa. Razvoj pod delovnim naslovom Anti-LINGO-1 švicarskega podjetja Biogen, največjega proizvajalca zdravil za zdravljenje multiple skleroze, trenutno poteka v 2. fazi kliničnih preskušanj. Zdravilo je monoklonsko protitelo, ki se lahko specifično veže na protein LINGO-1, kar preprečuje proces mielinizacije in nastanek novih aksonov. V skladu s tem, če je ta protein "izklopljen", se mielin začne obnavljati.
V poskusih na živalih je uporaba novega zdravila povzročila 90-odstotno remielinizacijo. Pri bolnikih z multiplo sklerozo, ki jemljejo Anti-LINGO-1, se trenutno izboljša prevodnost vidnega živca. Vendar pa bodo popolni rezultati kliničnih preskušanj na bolnikih prejeti šele leta 2016.