Les humains et les vertébrés ont un plan structurel unique et sont représentés par la partie centrale - le cerveau et la moelle épinière, ainsi que la section périphérique - les nerfs s'étendant des organes centraux, qui sont des processus de cellules nerveuses - les neurones.
Caractéristiques des cellules neurogliales
Comme nous l'avons déjà dit, la gaine de myéline des dendrites et des axones est formée de structures spéciales caractérisées par un faible degré de perméabilité aux ions sodium et calcium, et n'ayant donc que des potentiels de repos (elles ne peuvent pas conduire les impulsions nerveuses et remplir des fonctions d'isolation électrique).
Ces structures sont appelées Celles-ci comprennent :
- les oligodendrocytes ;
- astrocytes fibreux;
- cellules d'épendyme;
- astrocytes plasmatiques.
Tous sont formés à partir de la couche externe de l'embryon - l'ectoderme et ont un nom commun - la macroglie. Les cellules gliales des nerfs sympathique, parasympathique et somatique sont représentées par les cellules de Schwann (neurolemmocytes).
La structure et les fonctions des oligodendrocytes
Ils font partie du système nerveux central et sont des cellules macrogliales. La myéline étant une structure protéique-lipidique, elle contribue à augmenter la vitesse d'excitation. Les cellules elles-mêmes forment une couche électriquement isolante de terminaisons nerveuses dans le cerveau et la moelle épinière, se formant déjà dans la période de développement intra-utérin. Leurs processus enveloppent les neurones, ainsi que les dendrites et les axones, dans les plis de leur plasmalemme externe. Il s'avère que la myéline est le principal matériau électriquement isolant qui délimite les processus nerveux des nerfs mixtes.

et leurs caractéristiques
La gaine de myéline des nerfs du système périphérique est formée de neurolemmocytes (cellules de Schwann). Leur particularité est qu'ils sont capables de former une gaine protectrice d'un seul axone et ne peuvent pas former de processus, comme cela est inhérent aux oligodendrocytes.
Entre les cellules de Schwann à une distance de 1-2 mm, il y a des zones dépourvues de myéline, les soi-disant nœuds de Ranvier. À travers eux, les impulsions électriques sont effectuées de manière spasmodique dans l'axone.
Les lemmocytes sont capables de réparer les fibres nerveuses et également de fonctionner. À la suite d'aberrations génétiques, les cellules de la membrane des lemmocytes commencent une division et une croissance mitotiques incontrôlées, à la suite desquelles des tumeurs - schwannomes (neurinomes) se développent dans diverses parties du système nerveux.
Le rôle de la microglie dans la destruction de la structure de la myéline
Les microglies sont des macrophages capables de phagocytose et capables de reconnaître diverses particules pathogènes - les antigènes. Grâce aux récepteurs membranaires, ces cellules gliales produisent des enzymes - des protéases, ainsi que des cytokines, par exemple l'interleukine 1. C'est un médiateur du processus inflammatoire et de l'immunité.
La gaine de myéline, dont la fonction est d'isoler le cylindre axial et d'améliorer la conduction de l'influx nerveux, peut être endommagée par l'interleukine. En conséquence, le nerf est "nu" et le taux d'excitation est fortement réduit.

De plus, les cytokines, en activant des récepteurs, provoquent un transport excessif d'ions calcium dans le corps du neurone. Les protéases et les phospholipases commencent à décomposer les organites et les processus des cellules nerveuses, ce qui conduit à l'apoptose - la mort de cette structure.
Il s'effondre, se désintègre en particules, qui sont dévorées par les macrophages. Ce phénomène est appelé excitotoxicité. Il provoque la dégénérescence des neurones et de leurs terminaisons, conduisant à des maladies telles que la maladie d'Alzheimer et la maladie de Parkinson.
Fibres nerveuses de la pulpe
Si les processus des neurones - dendrites et axones, sont recouverts d'une gaine de myéline, ils sont appelés pulpeux et innervent les muscles squelettiques, pénétrant dans la section somatique du système nerveux périphérique. Les fibres non myélinisées forment le système nerveux autonome et innervent les organes internes.

Les processus pulpeux ont un diamètre plus grand que les processus non charnus et se forment comme suit: les axones plient la membrane plasmique des cellules gliales et forment des mésaxons linéaires. Ensuite, ils s'allongent et les cellules de Schwann s'enroulent à plusieurs reprises autour de l'axone, formant des couches concentriques. Le cytoplasme et le noyau du lemmocyte se déplacent vers la région de la couche externe, appelée neurilemme ou membrane de Schwann.
La couche interne du lemmocyte est constituée d'un mésoxon en couches et s'appelle la gaine de myéline. Son épaisseur dans différentes parties du nerf n'est pas la même.
Comment réparer la gaine de myéline
Considérant le rôle de la microglie dans le processus de démyélinisation nerveuse, nous avons constaté que sous l'action des macrophages et des neurotransmetteurs (par exemple, les interleukines), la myéline est détruite, ce qui entraîne à son tour une détérioration de la nutrition des neurones et une perturbation de la transmission. de l'influx nerveux le long des axones.
Cette pathologie provoque l'apparition de phénomènes neurodégénératifs : détérioration des processus cognitifs, principalement de la mémoire et de la pensée, apparition d'une altération de la coordination des mouvements corporels et de la motricité fine.

En conséquence, une invalidité complète du patient est possible, ce qui survient à la suite de maladies auto-immunes. Par conséquent, la question de savoir comment restaurer la myéline est actuellement particulièrement aiguë. Ces méthodes comprennent principalement une alimentation équilibrée en protéines et en lipides, un mode de vie approprié et l'absence de mauvaises habitudes. Dans les cas graves de maladies, un traitement médicamenteux est utilisé pour restaurer le nombre de cellules gliales matures - les oligodendrocytes.
Le système nerveux des humains et des vertébrés a un plan structurel unique et est représenté par la partie centrale - le cerveau et la moelle épinière, ainsi que la section périphérique - partant des organes centraux par les nerfs, qui sont des processus de cellules nerveuses - les neurones.
Leur combinaison forme le tissu nerveux dont les principales fonctions sont l'excitabilité et la conductivité. Ces propriétés s'expliquent principalement par les caractéristiques structurelles des enveloppes des neurones et de leurs processus, constitués d'une substance appelée myéline. Dans cet article, nous examinerons la structure et les fonctions de ce composé, ainsi que les moyens possibles de le restaurer.
Pourquoi les neurocytes et leurs processus sont-ils recouverts de myéline
Ce n'est pas un hasard si les dendrites et les axones ont une couche protectrice constituée de complexes protéines-lipides. Le fait est que la violation est un processus biophysique basé sur de faibles impulsions électriques. Si du courant électrique traverse le fil, celui-ci doit être recouvert d'un matériau isolant afin de réduire la dispersion des impulsions électriques et d'éviter une diminution de l'intensité du courant. La gaine de myéline remplit les mêmes fonctions dans la fibre nerveuse. De plus, c'est un support et fournit également de l'énergie à la fibre.
La composition chimique de la myéline
Comme la plupart des membranes cellulaires, il a une nature lipoprotéique. De plus, la teneur en matières grasses ici est très élevée - jusqu'à 75% et les protéines - jusqu'à 25%. La myéline contient également une petite quantité de glycolipides et de glycoprotéines. Sa composition chimique diffère dans les nerfs rachidiens et crâniens.
Dans le premier, il y a une teneur élevée en phospholipides - jusqu'à 45%, et le reste tombe sur le cholestérol et les cérébrosides. La démyélinisation (c'est-à-dire le remplacement de la myéline par d'autres substances dans les processus nerveux) conduit à des maladies auto-immunes graves telles que, par exemple, la sclérose en plaques.
D'un point de vue chimique, ce processus ressemblera à ceci : la gaine de myéline des fibres nerveuses change de structure, ce qui se manifeste principalement par une diminution du pourcentage de lipides par rapport aux protéines. De plus, la quantité de cholestérol diminue et la teneur en eau augmente. Et tout cela conduit à un remplacement progressif de la myéline, qui contient des oligodendrocytes ou cellules de Schwann, des macrophages, des astrocytes et du liquide intercellulaire. Le résultat de tels changements biochimiques sera une forte diminution de la capacité des axones à conduire l'excitation jusqu'au blocage complet du passage de l'influx nerveux.
Caractéristiques des cellules neurogliales
Comme nous l'avons déjà dit, la gaine de myéline des dendrites et des axones est formée de structures spéciales qui se caractérisent par un faible degré de perméabilité aux ions sodium et calcium, et n'ont donc que des potentiels de repos (ils ne peuvent pas conduire les impulsions nerveuses et remplir des fonctions d'isolation électrique ). Ces structures sont appelées cellules gliales. Ceux-ci inclus:
- les oligodendrocytes ;
- astrocytes fibreux;
- cellules épendymaires;
- astrocytes plasmatiques.
Tous sont formés à partir de la couche externe de l'embryon - l'ectoderme et ont un nom commun - la macroglie. Les cellules gliales des nerfs somatiques sympathiques et parasympathiques sont représentées par les cellules de Schwann (neurolemmocytes).
La structure et les fonctions des oligodendrocytes
Ils font partie du système nerveux central et sont des cellules macrogliales. La myéline étant une structure protéique-lipidique, elle contribue à augmenter la vitesse d'excitation. Les cellules elles-mêmes forment une couche électriquement isolante de terminaisons nerveuses dans le cerveau et la moelle épinière, se formant déjà dans la période de développement intra-utérin. Leurs processus enveloppent les neurones, ainsi que les dendrites et les axones, dans les plis de leur plasmalemme externe. Il s'avère que la myéline est le principal matériau électriquement isolant qui délimite les processus nerveux des nerfs mixtes.
Cellules de Schwann et leurs caractéristiques
La gaine de myéline des nerfs du système périphérique est formée de neurolemmocytes (cellules de Schwann). Leur particularité est qu'ils sont capables de former une gaine protectrice d'un seul axone et ne peuvent pas former de processus, comme cela est inhérent aux oligodendrocytes. Entre les cellules de Schwann à une distance de 1-2 mm, il y a des zones dépourvues de myéline, les soi-disant nœuds de Ranvier. Derrière lui, des impulsions électriques sont effectuées de manière spasmodique dans l'axone. Les lemmocytes sont capables de réparer les fibres nerveuses et remplissent également une fonction trophique. À la suite d'aberrations génétiques, les cellules de l'enveloppe des lemmocytes commencent une division et une croissance mitotiques incontrôlées, à la suite desquelles des tumeurs, les schwannomes (neurinomes), se développent dans différentes parties du système nerveux.
Le rôle de la microglie dans la destruction de la structure de la myéline
Les microglies sont des macrophages capables de phagocytose et capables de reconnaître diverses particules pathogènes - les antigènes. Grâce aux récepteurs membranaires, ces cellules gliales produisent des enzymes - des protéases, ainsi que des cytokines, par exemple l'interleukine 1. C'est un médiateur du processus inflammatoire et de l'immunité. La gaine de myéline, dont la fonction est d'isoler le cylindre axial et d'améliorer la conduction de l'influx nerveux, peut être endommagée par l'interleukine. En conséquence, le nerf est «exposé» et le taux de conduction d'excitation est fortement réduit.
De plus, les cytokines, en activant des récepteurs, provoquent un transport excessif d'ions calcium dans le corps du neurone. Les protéases et les phospholipases commencent à décomposer les organites et les processus des cellules nerveuses, ce qui conduit à l'apoptose - la mort de cette structure. Il s'effondre, se désintègre en particules, qui sont dévorées par les macrophages. Ce phénomène est appelé excitotoxicité. Il provoque la dégénérescence des neurones et de leurs terminaisons, conduisant à des maladies telles que la maladie d'Alzheimer et la maladie de Parkinson.
Fibres nerveuses de la pulpe
Si les processus des neurones - dendrites et axones, sont recouverts d'une gaine de myéline, ils sont appelés pulpeux et innervent les muscles squelettiques, pénétrant dans la section somatique du système nerveux périphérique. Les fibres non myélinisées forment le système nerveux autonome et innervent les organes internes.
Les processus pulpeux ont un diamètre plus grand que les processus non pulmonaires et se forment comme suit : les axones courbent la membrane plasmique des cellules gliales et forment des mésaxons linéaires. Ils grossissent ensuite et les cellules de Schwann s'enroulent à plusieurs reprises autour de l'axone, formant des couches concentriques. Le cytoplasme et le noyau du lemmocyte se déplacent vers la région de la couche externe, appelée neurilemme ou membrane de Schwann. La couche interne du lemmocyte est constituée d'un mésoxon en couches et s'appelle la gaine de myéline. Son épaisseur dans différentes parties du nerf n'est pas la même.
Comment réparer la gaine de myéline
Compte tenu du rôle de la microglie dans le processus de démyélinisation nerveuse, nous avons constaté que sous l'action des macrophages et des neurotransmetteurs (par exemple, les interleukines), la myéline est détruite, ce qui entraîne à son tour une détérioration de la nutrition des neurones et une violation de la transmission. de l'influx nerveux le long des axones. Cette pathologie provoque l'apparition de phénomènes neurodégénératifs : détérioration des processus cognitifs, principalement de la mémoire et de la pensée, apparition d'une altération de la coordination des mouvements corporels et de la motricité fine.
En conséquence, une invalidité complète du patient est possible, ce qui survient à la suite de maladies auto-immunes. Par conséquent, la question de savoir comment restaurer la myéline est actuellement particulièrement aiguë. Ces méthodes comprennent, tout d'abord, une alimentation équilibrée en protéines et en lipides, une bonne hygiène de vie et l'absence de mauvaises habitudes. Dans les cas graves de maladies, un traitement médicamenteux est utilisé pour restaurer le nombre de cellules gliales matures - les oligodendrocytes.
Date de parution : 26/05/17Le système nerveux central (SNC) est un mécanisme unique responsable de la perception du monde environnant et des réflexes, ainsi que du contrôle du système des organes et tissus internes. Le dernier point est réalisé par la partie périphérique du système nerveux central à l'aide de cellules spéciales appelées neurones. Le tissu nerveux en est constitué, qui sert à transmettre les impulsions.
Les processus provenant du corps du neurone sont entourés d'une couche protectrice qui nourrit les fibres nerveuses et accélère la transmission des impulsions, et cette protection s'appelle la gaine de myéline. Tout signal transmis à travers les fibres nerveuses ressemble à une décharge de courant, et c'est leur couche externe qui ne permet pas à sa force de diminuer.
Si la gaine de myéline est endommagée, la perception complète dans cette partie du corps est perdue, mais la cellule peut survivre et les dommages guérissent avec le temps. Avec des blessures suffisamment graves, des médicaments conçus pour restaurer les fibres nerveuses comme Milgamma, Copaxone et autres seront nécessaires. Sinon, le nerf finira par mourir et la perception diminuera. Les maladies caractérisées par ce problème comprennent la radiculopathie, la polyneuropathie, etc., mais les médecins considèrent la sclérose en plaques (SEP) comme le processus pathologique le plus dangereux. Malgré son nom étrange, la maladie n'a rien à voir avec la définition directe de ces mots et signifie "cicatrices multiples" en traduction. Ils se produisent sur la gaine de myéline de la moelle épinière et du cerveau en raison d'une défaillance immunitaire. La SEP est donc une maladie auto-immune. Au lieu de fibres nerveuses, une cicatrice apparaît au site du foyer, constituée de tissu conjonctif, à travers lequel l'impulsion ne peut plus passer correctement.
Est-il possible de restaurer d'une manière ou d'une autre le tissu nerveux endommagé ou restera-t-il pour toujours dans un état paralysé? Les médecins ne peuvent toujours pas y répondre avec précision et n'ont pas encore mis au point un médicament à part entière pour restaurer la sensibilité des terminaisons nerveuses. Au lieu de cela, il existe divers médicaments qui peuvent réduire le processus de démyélinisation, améliorer la nutrition des zones endommagées et activer la régénération de la gaine de myéline.
Milgamma est un neuroprotecteur pour restaurer le métabolisme à l'intérieur des cellules, ce qui permet de ralentir le processus de destruction de la myéline et de démarrer sa régénération. Le médicament est à base de vitamines du groupe B, à savoir :
- Thiamine (B1). Il est essentiel pour l'absorption du sucre dans le corps et l'énergie. En cas de carence aiguë en thiamine chez une personne, le sommeil est perturbé et la mémoire se détériore. Il devient nerveux et parfois déprimé, comme dans la dépression. Dans certains cas, il existe des symptômes de paresthésie (chair de poule, diminution de la sensibilité et picotements au bout des doigts) ;
- Pyridoxine (B6). Cette vitamine joue un rôle important dans la production d'acides aminés, ainsi que de certaines hormones (dopamine, sérotonine, etc.). Malgré de rares cas de manque de pyridoxine dans l'organisme, du fait de sa carence, une diminution des capacités mentales et un affaiblissement des défenses immunitaires sont possibles ;
- Cyanocobalamine (B12). Il sert à améliorer la conductivité des fibres nerveuses, ce qui améliore la sensibilité, ainsi qu'à améliorer la synthèse sanguine. Avec un manque de cyanocobalamine, une personne développe des hallucinations, une démence (démence), il y a des perturbations du rythme cardiaque et des paresthésies.
Grâce à cette composition, Milgama est capable d'arrêter l'oxydation des cellules par les radicaux libres (substances réactives), ce qui affectera la restauration de la sensibilité des tissus et des terminaisons nerveuses. Après une cure de prise de comprimés, il y a une diminution des symptômes et une amélioration de l'état général, et le médicament doit être pris en 2 étapes. Dans le premier, vous devrez faire au moins 10 injections, puis passer aux comprimés (Milgamma compositum) et les prendre 3 fois par jour pendant 1,5 mois.

Le sulfate de stafaglabrine est utilisé depuis longtemps pour restaurer la sensibilité des tissus et des fibres nerveuses elles-mêmes. La plante dont les racines sont extraites de ce médicament ne pousse que dans les climats subtropicaux et tropicaux, par exemple au Japon, en Inde et en Birmanie, et s'appelle Stephania lisse. Il existe des cas d'obtention de sulfate de Stafaglabrine en laboratoire. Cela est peut-être dû au fait que stephania lisse peut être cultivée en culture en suspension, c'est-à-dire en position suspendue dans des flacons en verre contenant du liquide. En soi, le médicament est un sel de sulfate, qui a un point de fusion élevé (plus de 240 ° C). Il fait référence à la stéfarine, un alcaloïde (composé contenant de l'azote), qui est considérée comme la base de la proaporphine.
Le sulfate de stefaglabrine sert à réduire l'activité des enzymes de la classe des hydrolases (cholinestérase) et à améliorer le tonus des muscles lisses présents dans les parois des vaisseaux sanguins, des organes (creux à l'intérieur) et des ganglions lymphatiques. On sait également que le médicament est légèrement toxique et peut réduire la tension artérielle. Autrefois, le médicament était utilisé comme agent anticholinestérasique, mais les scientifiques sont ensuite arrivés à la conclusion que le sulfate de stefaglabrine est un inhibiteur de l'activité de croissance du tissu conjonctif. Il s'ensuit qu'il retarde son développement et que les cicatrices ne se forment pas sur les fibres nerveuses. C'est pourquoi le médicament a commencé à être activement utilisé pour endommager le SNP.
Au cours de la recherche, les experts ont pu observer la croissance des cellules de Schwann, qui produisent de la myéline dans le système nerveux périphérique. Ce phénomène signifie que sous l'influence du médicament, le patient améliore sensiblement la conduction de l'impulsion le long de l'axone, puisque la gaine de myéline a recommencé à se former autour de lui. Depuis l'obtention des résultats, le médicament est devenu un espoir pour de nombreuses personnes diagnostiquées avec des pathologies démyélinisantes incurables.

Il ne sera pas possible de résoudre le problème de la pathologie auto-immune uniquement en restaurant les fibres nerveuses. En effet, peu importe le nombre de foyers de dommages à éliminer, le problème reviendra, car le système immunitaire réagit à la myéline comme un corps étranger et la détruit. À ce jour, il est impossible d'éliminer un tel processus pathologique, mais on ne peut plus se demander si les fibres nerveuses sont restaurées ou non. Les gens sont laissés pour maintenir leur état en supprimant le système immunitaire et en utilisant des médicaments comme le sulfate de Stefaglabrin pour maintenir leur santé.
Le médicament ne peut être utilisé que par voie parentérale, c'est-à-dire par les intestins, par exemple par injection. La posologie dans ce cas ne doit pas dépasser 7-8 ml d'une solution à 0,25% par jour pour 2 injections. À en juger par le temps, la gaine de myéline et les terminaisons nerveuses sont généralement restaurées dans une certaine mesure après 20 jours, puis vous avez besoin d'une pause et vous pouvez comprendre combien de temps cela va durer, après en avoir entendu parler par le médecin. Selon les médecins, le meilleur résultat peut être obtenu au détriment de faibles doses, car les effets secondaires se développent beaucoup moins fréquemment et l'efficacité du traitement augmente.
Dans des conditions de laboratoire, à temps pour des expériences sur des rats, il a été constaté qu'avec une concentration du médicament sulfate de stéfaglabrine de 0,1 à 1 mg / kg, le traitement est plus rapide que sans lui. Le cours de la thérapie s'est terminé plus tôt, par rapport aux animaux qui n'ont pas pris ce médicament. Après 2-3 mois, les fibres nerveuses des rongeurs ont été presque complètement restaurées et l'impulsion a été transmise le long du nerf sans délai. Chez les sujets expérimentaux qui ont été traités sans ce médicament, la récupération a duré environ six mois et toutes les terminaisons nerveuses ne sont pas revenues à la normale.
Copaxon

La sclérose en plaques est incurable, mais il existe des médicaments qui peuvent réduire l'effet du système immunitaire sur la gaine de myéline, et Copaxone en fait partie. L'essence des maladies auto-immunes est que le système immunitaire détruit la myéline située sur les fibres nerveuses. De ce fait, la conductivité des impulsions s'aggrave et Copaxone est capable de changer l'objectif du système de défense de l'organisme en lui-même. Les fibres nerveuses restent intactes, mais si les cellules du corps ont déjà absorbé l'érosion de la gaine de myéline, le médicament pourra les repousser. Ce phénomène se produit en raison du fait que le médicament a une structure très similaire à la myéline, de sorte que le système immunitaire y porte son attention.
Le médicament est capable non seulement d'attaquer le système de défense de l'organisme, mais également de produire des cellules spéciales du système immunitaire pour réduire l'intensité de la maladie, appelées lymphocytes Th2. Le mécanisme de leur influence et de leur formation n'a pas encore été correctement étudié, mais il existe diverses théories. Il existe une opinion parmi les experts selon laquelle les cellules dendritiques de l'épiderme sont impliquées dans la synthèse des lymphocytes Th2.
Les lymphocytes suppresseurs (mutés) développés, pénétrant dans le sang, pénètrent rapidement dans la partie du système nerveux où se trouve le foyer de l'inflammation. Ici, les lymphocytes Th2, sous l'influence de la myéline, produisent des cytokines, c'est-à-dire des molécules anti-inflammatoires. Ils commencent à soulager progressivement l'inflammation dans cette partie du cerveau, améliorant ainsi la sensibilité des terminaisons nerveuses.
L'avantage du médicament n'est pas seulement pour le traitement de la maladie elle-même, mais également pour les cellules nerveuses elles-mêmes, car Copaxone est un neuroprotecteur. L'effet protecteur se manifeste par la stimulation de la croissance des cellules cérébrales et l'amélioration du métabolisme des lipides. La gaine de myéline est principalement constituée de lipides et, dans de nombreux processus pathologiques associés à des lésions des fibres nerveuses, leur oxydation se produit, de sorte que la myéline est endommagée. Le médicament Copaxone est capable d'éliminer ce problème, car il augmente l'antioxydant naturel du corps (acide urique). En raison de quoi le niveau d'acide urique augmente n'est pas connu, mais ce fait a été prouvé au cours de nombreuses expériences.
Le médicament sert à protéger les cellules nerveuses et à réduire la gravité et la fréquence des exacerbations. Il peut être combiné avec des médicaments sulfate de Stefaglabrin et Milgamma.
La gaine de myéline commencera à se rétablir en raison de la croissance accrue des cellules de Schwann, et Milgamma améliorera le métabolisme intracellulaire et renforcera l'effet des deux médicaments. Il est strictement interdit de les utiliser seuls ou de modifier le dosage de leur propre chef.
Est-il possible de restaurer les cellules nerveuses et combien de temps cela prendra, seul un spécialiste peut répondre, en se concentrant sur les résultats de l'examen. Il est interdit de prendre seul des médicaments pour améliorer la sensibilité des tissus, car la plupart d'entre eux ont une base hormonale, ce qui signifie qu'ils sont difficiles à tolérer par l'organisme.
FIBRES NERVEUSES
Les fibres nerveuses sont des processus de neurones recouverts de gaines gliales. Il existe deux types de fibres nerveuses - non myélinisées et myélinisées. Les deux types consistent en un processus situé au centre d'un neurone (un cylindre axial) entouré d'une gaine de cellules oligodendroglia (dans le SNP, ils sont appelés lemmocytes ou cellules de Schwann).
fibres nerveuses non myélinisées chez un adulte, ils se situent principalement dans le système nerveux autonome et se caractérisent par une vitesse relativement faible de conduction de l'influx nerveux (0.5-2 SP). Ils sont formés en immergeant le cylindre axial (axone) dans le cytoplasme des lemmocytes, qui se présentent sous la forme de brins. Dans ce cas, le plasmolemme du lemmocyte se plie, entourant l'axone, et forme une duplication - le mésaxon (Fig. 14-7). Souvent, dans le cytoplasme d'un lemmocyte, il peut y avoir jusqu'à 10-20 cylindres d'essieux. Une telle fibre ressemble à un câble électrique et est donc appelée fibre de type câble. La surface de la fibre est recouverte d'une membrane basale. Dans le SNC, notamment au cours de son développement, on décrit des fibres amyéliniques, constituées d'un axone « nu », dépourvu de gaine de lemmocytes.
Riz. 14-7. Formation de fibres nerveuses myélinisées (1-3) et non myélinisées (4) dans le système nerveux périphérique. La fibre nerveuse est formée en immergeant l'axone (A) de la cellule nerveuse dans le cytoplasme du lemmocyte (LC). Lorsqu'une fibre de myéline se forme, une duplication du plasmolemme LC - le mésaxon (MA) - est enroulée autour de A, formant des spires de la gaine de myéline (MO). Dans la fibre sans myéline représentée sur la figure, plusieurs A sont immergés dans le cytoplasme de la LC (fibre de type câble). Je suis le noyau du LC.

fibres nerveuses myélinisées trouvés dans le SNC et le SNP et se caractérisent par une vitesse élevée de conduction de l'influx nerveux (5-120 SP). Les fibres myélinisées sont généralement plus épaisses que les fibres non myélinisées et contiennent des cylindres axiaux de plus grand diamètre. Dans la fibre de myéline, le cylindre axial est directement entouré d'une gaine de myéline spéciale, autour de laquelle se trouve une fine couche qui comprend le cytoplasme et le noyau du lemmocyte - le neurolemme (Fig. 14-8 et 14-9). À l'extérieur, la fibre est également recouverte d'une membrane basale. La gaine de myéline contient de fortes concentrations de lipides et est intensément colorée avec de l'acide osmique, ayant l'apparence d'une couche homogène au microscope optique, mais au microscope électronique, on constate qu'elle résulte de la fusion de nombreux (jusqu'à 300) bobines à membrane (plaques).
Riz. 14-8. La structure de la fibre nerveuse myélinisée. La fibre de myéline est constituée d'un cylindre axial, ou axone (A), directement entouré d'une gaine de myéline (MO) et d'un neurolemme (NL), comprenant le cytoplasme (CL) et le noyau des lemmocytes (NL). À l'extérieur, la fibre est recouverte d'une membrane basale (BM). Les zones de MO, dans lesquelles les espaces entre les tours de myéline sont conservés, remplis de CL et donc non colorés à l'osmium, ont la forme d'encoches de myéline (MN).
Formation de la gaine de myéline se produit lors de l'interaction du cylindre axial et des cellules oligodendroglia avec quelques différences dans le SNP et le SNC.
Formation de la gaine de myéline dans le SNP : l'immersion du cylindre axial dans le lemmocyte s'accompagne de la formation d'un long mésaxon, qui commence à tourner autour de l'axone, formant les premières spires disposées de manière lâche de la gaine de myéline (voir Fig. 14-7). Au fur et à mesure que le nombre de tours (plaques) augmente au cours du processus de maturation de la myéline, ils sont disposés de plus en plus densément et fusionnent partiellement; les espaces entre eux, remplis du cytoplasme du lemmocyte, ne sont conservés que dans des zones séparées qui ne sont pas colorées d'osmium - encoches de myéline (Schmidt-Lanterman). Lors de la formation de la gaine de myéline, le cytoplasme et le noyau du lemmocyte sont poussés à la périphérie de la fibre, formant le neurolemme. La gaine de myéline a un trajet discontinu sur toute la longueur de la fibre.

Riz. 14-9. Organisation ultrastructurale de la fibre nerveuse myélinisée. Autour de l'axone (A) se trouvent des spires de la gaine de myéline (MMO), recouvertes extérieurement d'un neurolemme, et qui comprennent le cytoplasme (CL) et le noyau du lemmocyte (NL). La fibre est entourée à l'extérieur par une membrane basale (BM). CL, en plus du neurolemme, forme une feuille interne (IL) directement adjacente à A (située entre elle et le SMO), elle est également contenue dans la zone correspondant à la bordure des lemmocytes voisins - l'interception nodale (NC), où la gaine de myéline est absente et dans les zones d'empilement lâche de l'OMM - encoches de myéline (MN).
Interceptions nodales (Ranvier)- des zones dans la région du bord des lemmocytes voisins, dans lesquelles la gaine de myéline est absente et l'axone n'est recouvert que par les processus interdigités des lemmocytes voisins (voir Fig. 14-9). Les interceptions nodales sont répétées le long du parcours de la fibre de myéline avec un intervalle égal, en moyenne, à 1-2 mm. Dans la région du nœud nodal, l'axone se dilate souvent et son plasmolemme contient de nombreux canaux sodiques (qui sont absents à l'extérieur des nœuds sous la gaine de myéline).
Propagation de la dépolarisation dans la fibre de myéline effectué en sauts d'interception en interception (saltatoire). La dépolarisation dans la région d'une jonction nodale s'accompagne de sa propagation passive rapide le long de l'axone jusqu'à la jonction suivante (puisque la fuite de courant dans la région internodale est minime en raison des propriétés isolantes élevées de la myéline). Dans la zone de la prochaine interception, l'impulsion provoque l'activation des canaux ioniques existants et une nouvelle zone de dépolarisation locale apparaît, etc.
Formation de la gaine de myéline dans le SNC : le cylindre axial ne s'enfonce pas dans le cytoplasme de l'oligodendrocyte, mais est recouvert par son processus plat, qui tourne ensuite autour de lui, perdant le cytoplasme, et ses bobines se transforment en plaques de la gaine de myéline

coudes (Fig. 14-10). Contrairement aux cellules de Schwann, un oligodendrocyte du SNC avec ses processus peut participer à la myélinisation de nombreuses (jusqu'à 40-50) fibres nerveuses. Les sites axonaux dans la zone des nœuds de Ranvier dans le SNC ne sont pas recouverts par le cytoplasme des oligodendrocytes.
Riz. 14-10. La formation de fibres de myéline par les oligodendrocytes dans le SNC. 1 - l'axone (A) du neurone est recouvert d'un processus plat (PO) de l'oligodendrocyte (ODC), dont les spires se transforment en plaques de la gaine de myéline (MO). 2 - un ODC avec ses processus peut participer à la myélinisation de nombreux A. Les zones A dans la zone des interceptions nodales (NC) ne sont pas couvertes par le cytoplasme de l'ODC.
Violation de la formation et des dommages de la myéline formée sous-tendent un certain nombre de maladies graves du système nerveux. La myéline dans le SNC peut être une cible de dommages auto-immuns Lymphocytes T et les macrophages avec sa destruction (démyélinisation). Ce processus se déroule activement dans la sclérose en plaques, une maladie grave de nature incertaine (probablement virale), associée à un trouble de diverses fonctions, au développement d'une paralysie et à une perte de sensibilité. La nature des troubles neurologiques est déterminée par la topographie et la taille des zones endommagées. Avec certains troubles métaboliques, il existe des troubles de la formation de la myéline - la leucodystrophie, qui se manifestent dans l'enfance par de graves lésions du système nerveux.
Classification des fibres nerveuses
Classification des fibres nerveuses repose sur des différences dans leur structure et leur fonction (vitesse de l'influx nerveux). Il existe trois principaux types de fibres nerveuses :
1. Fibres de type A - épais, myélinisé, avec des interceptions nodales très éloignées. Conduire des impulsions à grande vitesse
(15-120 m/s); subdivisé en 4 sous-types (α, β, γ, δ) de diamètre et de vitesse de conduction des impulsions décroissants.
2. Fibres de type B - épaisseur moyenne, myéline, diamètre plus petit,
que les fibres de type A, avec une gaine de myéline plus fine et une vitesse de conduction de l'influx nerveux plus faible (5-15 m/s).
3. Fibres de type C - fines, non myélinisées, conduire des impulsions à une vitesse relativement faible(0,5-2 m/s).
Régénération des fibres nerveuses dans le SNP comprend une séquence complexe de processus se déroulant naturellement au cours de laquelle le processus neuronal interagit activement avec les cellules gliales. La régénération proprement dite des fibres suit une série de changements réactifs provoqués par leur endommagement.
Modifications réactives de la fibre nerveuse après sa section. Au cours de la 1ère semaine après la coupe de la fibre nerveuse, se développe une dégénérescence ascendante de la partie proximale (la plus proche du corps du neurone) de l'axone, au bout de laquelle se forme une extension (flacon de rétraction). La gaine de myéline dans la zone endommagée se désintègre, le corps du neurone gonfle, le noyau se déplace vers la périphérie, la substance chromatophile se dissout (Fig. 14-11).
Dans la partie distale de la fibre, après sa section transversale, on note une dégénérescence descendante avec destruction complète de l'axone, dégradation de la myéline et phagocytose ultérieure des détritus par les macrophages et la glie.
Transformations structurales lors de la régénération de la fibre nerveuse. Après 4-6 semaines. la structure et la fonction du neurone sont restaurées, de fines branches (cônes de croissance) commencent à se développer à partir du ballon de rétraction en direction de la partie distale de la fibre. Les cellules de Schwann dans la partie proximale de la fibre prolifèrent, formant des rubans (Büngner) parallèles au trajet de la fibre. Dans la partie distale de la fibre, les cellules de Schwann persistent également et se divisent de manière mitotique, formant des rubans qui se connectent à des formations similaires dans la partie proximale.
L'axone en régénération croît dans la direction distale à une vitesse de 3 à 4 mm/jour. le long des bandes Büngner, qui jouent un rôle de soutien et de guidage ; Les cellules de Schwann forment une nouvelle gaine de myéline. Les collatéraux et les terminaux d'axones sont restaurés en quelques mois.

Riz. 14-11. Régénération de la fibre nerveuse myélinisée (selon R.Krstic, 1985, avec modifications). 1 - après section de la fibre nerveuse, la partie proximale de l'axone (A) subit une dégénérescence ascendante, la gaine de myéline (MO) dans la zone lésée se désagrège, le péricaryon (PC) du neurone gonfle, le noyau se déplace à la périphérie, la substance chromatophile (CS) se désagrège (2). La partie distale associée à l'organe innervé (dans l'exemple donné, le muscle squelettique) subit une dégénérescence descendante avec destruction complète de A, désintégration de MO et phagocytose des détritus par les macrophages (MF) et la glie. Les lemmocytes (LC) persistent et se divisent de manière mitotique, formant des brins - les rubans de Büngner (LB), se connectant avec des formations similaires dans la partie proximale de la fibre (flèches fines). Après 4 à 6 semaines, la structure et la fonction du neurone sont restaurées, de fines branches poussent distalement à partir de la partie proximale A (flèche en gras), poussant le long du LB (3). À la suite de la régénération de la fibre nerveuse, la connexion avec l'organe cible (muscle) est restaurée et son atrophie causée par une innervation altérée régresse (4). En cas d'obstruction (P) sur la voie de régénération A (par exemple, une cicatrice du tissu conjonctif), les composants de la fibre nerveuse
forment un névrome traumatique (TN), qui consiste en la croissance des branches A et LC (5).
conditions de régénération sont : aucun dommage au corps du neurone, une petite distance entre les parties de la fibre nerveuse, l'absence de tissu conjonctif qui peut combler l'espace entre les parties de la fibre. Lorsqu'une obstruction se produit sur le chemin de l'axone en régénération, un névrome traumatique (amputation) se forme, qui consiste en un axone en croissance et des cellules de Schwann soudées dans le tissu conjonctif.
Il n'y a pas de régénération des fibres nerveuses dans le SNC : bien que les neurones du SNC aient la capacité de restaurer leurs processus, cela ne se produit pas, apparemment en raison de l'influence néfaste du microenvironnement. Après avoir endommagé un neurone, la microglie, les astrocytes et les macrophages hématogènes phagocytent les détritus dans la zone de la fibre détruite et les astrocytes en prolifération forment une cicatrice gliale dense à sa place.
FINS NERVEUSES
Terminaisons nerveuses- les dispositifs terminaux des fibres nerveuses. Selon leur fonction, ils sont divisés en trois groupes :
1) contacts interneuraux (synapses)- fournir une connexion fonctionnelle entre les neurones ;
2) terminaisons efférentes (effectrices)- transmettent les signaux du système nerveux aux organes exécutifs (muscles, glandes), sont présents sur les axones ;
3) terminaisons réceptrices (sensibles)perçoivent les irritations du milieu externe et interne, sont présentes sur les dendrites.
CONTACTS INTERNEURONEAUX (SYNAPSE)
Contacts interneuraux (synapses) divisé en électrique et chimique.
synapses électriques rare dans le SNC des mammifères; ils ont la structure de jonctions lacunaires, dans lesquelles les membranes des cellules connectées synaptiques (pré- et post-synaptiques) sont séparées par un espace de 2 nm de large percé de connexons. Ces derniers sont des tubes formés par des molécules de protéines et servent de canaux d'eau à travers lesquels de petites molécules et des ions peuvent être transportés d'une cellule à une autre.

un autre (voir chapitre 3). Lorsqu'un potentiel d'action se propageant à travers la membrane d'une cellule atteint la jonction lacunaire, un courant électrique circule passivement à travers la fente d'une cellule à l'autre. L'impulsion peut être transmise dans les deux sens et pratiquement sans délai.
Synapses chimiques- le type le plus courant chez les mammifères. Leur action repose sur la conversion d'un signal électrique en un signal chimique, qui est ensuite reconverti en signal électrique. La synapse chimique se compose de trois composants : la partie présynaptique, la partie postsynaptique et la fente synaptique (Fig. 14-12). La partie présynaptique contient un (neuro)transmetteur qui, sous l'influence d'un influx nerveux, est libéré dans la fente synaptique et, se liant aux récepteurs de la partie postsynaptique, provoque des modifications de la perméabilité ionique de sa membrane, ce qui conduit à sa dépolarisation (dans les synapses excitatrices) ou hyperpolarisation (dans les synapses inhibitrices). ). Les synapses chimiques diffèrent des synapses électriques par la conduction unilatérale des impulsions, un retard dans leur transmission (un retard synaptique de 0,2 à 0,5 ms) et la fourniture à la fois d'excitation et d'inhibition du neurone postsynaptique.
Riz. 14-12. La structure d'une synapse chimique. La partie présynaptique (PRSP) a la forme d'un bouton terminal (CB) et comprend : les vésicules synaptiques (SP), les mitochondries (MTX), les neurotubules (NT), les neurofilaments (NF), la membrane présynaptique (PRSM) avec compaction présynaptique (PRSU ). La partie postsynaptique (PSCH) comprend la membrane postsynaptique (POSM) avec le compactage postsynaptique (POSU). La fente synaptique (SC) contient des filaments intrasynaptiques (ISF).
1. partie présynaptique est formé par l'axone le long de son parcours (synapse passante) ou est une partie terminale étendue de l'axone (bourgeon terminal). Il contient des mitochondries, des aER, des neurofilaments, des neurotubules et des vésicules synaptiques d'un diamètre de 20 à 65 nm, qui contiennent le neurotransmetteur. La forme et la nature du contenu des vésicules dépendent des neurotransmetteurs qu'elles contiennent. Les vésicules légères rondes contiennent généralement de l'acétylcholine, des vésicules avec un centre compact et dense - la norépinéphrine, de grandes vésicules denses avec un bord sous-membranaire léger - des peptides. Les neurotransmetteurs sont produits dans le corps du neurone et sont transportés vers les terminaisons axonales par le mécanisme de transport rapide, où ils se déposent. En partie, les vésicules synaptiques se forment dans la synapse elle-même en se séparant des citernes de l'aER. Sur la face interne du plasmolemme, face à la fente synaptique (membrane présynaptique), se trouve un joint présynaptique formé par un réseau protéique hexagonal fibrillaire dont les cellules contribuent à une répartition uniforme des vésicules synaptiques à la surface de la membrane.
2. partie postsynaptique Il est représenté par une membrane postsynaptique contenant des complexes spéciaux de protéines intégrales - des récepteurs synaptiques qui se lient à un neurotransmetteur. La membrane est épaissie en raison de l'accumulation de matière protéique filamenteuse dense en dessous (compactage post-synaptique). Selon que la partie postsynaptique de la synapse interneuronale est la dendrite, le corps du neurone ou (moins souvent) son axone, les synapses sont divisées en axo-dendritiques, axosomatiques et axo-axonales, respectivement.
3. fente synaptique 20-30 nm de large contient parfois des filaments intrasynaptiques transversaux de glycoprotéine de 5 nm d'épaisseur, qui sont des éléments d'un glycocalyx spécialisé qui assurent des liaisons adhésives des parties pré- et post-synatiques, ainsi qu'une diffusion dirigée du médiateur.
Le mécanisme de transmission d'un influx nerveux dans une synapse chimique. Sous l'influence d'un influx nerveux, les canaux calciques voltage-dépendants de la membrane présynaptique sont activés; SA 2+ se précipite vers l'axone, les membranes des vésicules synaptiques en présence de Ca2+ fusionnent avec la membrane présynaptique, et leur contenu (médiateur) est libéré dans la fente synaptique par le mécanisme de l'exocytose. En agissant sur les récepteurs de la membrane postsynaptique, le médiateur provoque soit sa dépolarisation, l'émergence d'un potentiel d'action postsynaptique et la formation d'un influx nerveux, soit son hyperpigmentation.
polarisation, provoquant une réponse inhibitrice. Les médiateurs excitateurs, par exemple, sont l'acétylcholine et le glutamate, tandis que l'inhibition est médiée par le GABA et la glycine.
Après la fin de l'interaction du médiateur avec les récepteurs de la membrane postsynaptique, la majeure partie de son endocytose est capturée par la partie présynaptique, la plus petite partie est dispersée dans l'espace et capturée par les cellules gliales environnantes. Certains médiateurs (par exemple, l'acétylcholine) sont décomposés par des enzymes en composants qui sont ensuite capturés par la partie présynaptique. Les membranes des vésicules synaptiques intégrées dans la membrane présynaptique sont ensuite incorporées dans des vésicules tapissées d'endocytose et réutilisées pour former de nouvelles vésicules synaptiques.
En l'absence d'influx nerveux, la partie présynaptique libère de petites portions individuelles du médiateur, provoquant des potentiels miniatures spontanés dans la membrane postsynaptique.
FINS NERVEUSES EFFÉRENTES (EFFECTEURS)
Terminaisons nerveuses efférentes (effectrices) Selon la nature de l'organe innervé, ils sont divisés en moteurs et sécrétoires. Les terminaisons motrices se trouvent dans les muscles striés et lisses, sécrétoires - dans les glandes.
Terminaison neuromusculaire (jonction neuromusculaire, plaque motrice) - la terminaison motrice de l'axone du motoneurone sur les fibres des muscles somatiques striés - est constituée de la ramification terminale de l'axone, qui forme la partie présynaptique, une zone spécialisée sur la fibre musculaire, correspondant à la partie postsynaptique, et la fente synaptique les séparant (Fig. 14-13).
Dans les grands muscles qui développent une force importante, un axone, ramifié, innerve un grand nombre (des centaines et des milliers) de fibres musculaires. Au contraire, dans les petits muscles qui effectuent des mouvements fins (par exemple, les muscles externes de l'œil), chaque fibre ou un petit groupe d'entre elles est innervée par un axone séparé. Un motoneurone, avec les fibres musculaires qu'il innerve, forme une unité motrice.
partie présynaptique. Près de la fibre musculaire, l'axone perd sa gaine de myéline et donne naissance à plusieurs branches qui
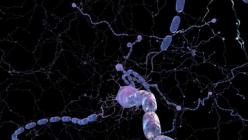
La sclérose en plaques est une autre preuve de l'imperfection de notre système immunitaire, qui parfois « devient fou » et commence à attaquer non pas un « ennemi » extérieur, mais les tissus de son propre corps. Dans cette maladie, les cellules du système immunitaire détruisent la gaine de myéline des fibres nerveuses, qui se forme lors du développement du corps à partir d'un certain type de cellules gliales - les cellules «de service» du système nerveux. La gaine de myéline recouvre les axones - de longs processus d'un neurone qui agissent comme des "fils" à travers lesquels se déplace l'influx nerveux. La gaine elle-même sert d'isolation électrique et, à la suite de sa destruction, le passage d'une impulsion le long de la fibre nerveuse ralentit de 5 à 10 fois.
Sur la photo, des accumulations de macrophages (couleur marron) sont visibles le long de la périphérie des plaques. Les macrophages sont attirés par la lésion et activés par d'autres cellules du système immunitaire - les lymphocytes T. Les macrophages activés phagocytent («mangent») la myéline mourante et, en outre, ils contribuent eux-mêmes à ses dommages, produisant des protéases, des molécules pro-inflammatoires et des espèces réactives de l'oxygène. (Immunohistochimie, marqueur macrophage - CD68).
Normalement, les cellules du système immunitaire, comme les autres cellules sanguines, ne peuvent pas pénétrer directement dans le tissu nerveux - elles ne sont pas autorisées par la soi-disant barrière hémato-encéphalique. Mais avec la sclérose en plaques, cette barrière devient franchissable : les lymphocytes « fous » accèdent aux neurones et à leurs axones, où ils commencent à attaquer les molécules de myéline, qui sont une structure protéino-lipidique multicouche complexe. Cela déclenche une cascade d'événements moléculaires conduisant à la destruction de la myéline et parfois des axones eux-mêmes.
La destruction de la myéline s'accompagne du développement d'une inflammation et d'une sclérose de la zone touchée, c'est-à-dire la formation d'une cicatrice de tissu conjonctif sous la forme d'une plaque qui remplace la gaine de myéline. En conséquence, dans cette zone, la fonction conductrice de l'axone est altérée. Les plaques sont localisées de manière diffuse, dispersées dans tout le système nerveux. C'est à cet agencement de lésions qu'est associé le nom même de la maladie - sclérose en plaques, qui n'a rien à voir avec la distraction ordinaire (celle dont on parle parfois dans la vie de tous les jours - "j'ai complètement la sclérose, J'ai encore tout oublié »).
Les symptômes de la sclérose en plaques varient et dépendent des nerfs touchés. Parmi eux figurent la paralysie, les problèmes d'équilibre, les troubles cognitifs, les modifications du fonctionnement des organes des sens (chez un quart des patients, le développement de la maladie commence par une déficience visuelle due à une névrite optique).
Le traitement moderne de la sclérose en plaques laisse beaucoup à désirer.
Il n'existe pas encore de traitement efficace, d'autant plus que les causes de cette maladie ne sont toujours pas connues, il n'y a que des données sur l'influence possible de l'environnement et de la prédisposition génétique. Pour le traitement, en plus de la thérapie symptomatique, qui peut soulager la douleur et réduire les spasmes musculaires, des préparations de glucocorticoïdes sont utilisées pour réduire l'inflammation, ainsi que des immunomodulateurs et des immunosuppresseurs visant à supprimer la "mauvaise" activité du système immunitaire. Tous ces remèdes peuvent ralentir le développement de la maladie et réduire la fréquence des exacerbations, mais ne guérissent pas complètement le patient. Aucun médicament ne peut réparer la myéline déjà endommagée.
Cependant, un tel médicament, visant spécifiquement à restaurer la myéline, et pas seulement à ralentir le processus pathologique, pourrait bientôt apparaître. Le développement sous le titre provisoire Anti-LINGO-1 de la société suisse Biogen, le plus grand fabricant de médicaments pour le traitement de la sclérose en plaques, fait actuellement l'objet d'essais cliniques de phase 2. Le médicament est un anticorps monoclonal qui peut se lier spécifiquement à la protéine LINGO-1, ce qui empêche le processus de myélinisation et la formation de nouveaux axones. En conséquence, si cette protéine est "désactivée", la myéline commence à récupérer.
Dans les expérimentations animales, l'utilisation du nouveau médicament a conduit à une remyélinisation de 90 %. Les patients atteints de sclérose en plaques prenant Anti-LINGO-1 ont actuellement une amélioration de la conduction du nerf optique. Cependant, les résultats complets des essais cliniques sur les patients ne seront reçus qu'en 2016.